Bisfenol A
| Bisfenol A Alerta sobre risco à saúde | |
|---|---|

| |
| |
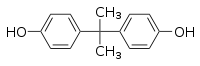
| Nome IUPAC | 4,4'-dihidroxi-2,2-difenilpropano |
| Outros nomes | BPA, 4,4'-(propano-2-ilideno)difenol, p, p'-isopropilidenobisfenol, 4,4´-isopropilidenodifenol 2,2-bis(4-hidroxifenil)propano |
| Identificadores | |
| Número CAS | |
| PubChem | |
| Número EINECS | |
| Número RTECS | SL6300000 |
| Propriedades | |
| Fórmula química | C15H16O2 |
| Massa molar | 228.28 g mol-1 |
| Aparência | Sólido. Flocos ou pó branco a castanho claro |
| Densidade | 1,20 g/cm³ [1] |
| Ponto de fusão |
155 a 156 °C[2] |
| Ponto de ebulição |
360 °C |
| Solubilidade em água | 300 mg·l−1 [1] |
| Solubilidade | solúvel em álcool[1] |
| Farmacologia | |
| Riscos associados | |
| NFPA 704 | |
| Frases R | R37, R41, R43, R62, R52 |
| Frases S | S2, S26, S36/37, S39, S46
, S61 |
| Ponto de fulgor | 227 °C |
| Temperatura de auto-ignição |
600 °C |
| Compostos relacionados | |
| Outros aniões/ânions | 2,2-Bis(4-aminofenil)propano (aminas no lugar das hidroxilas) Metoxibisfenol A (2,2-bis(4-metoxifenil) propano ou MBPA) |
| Bisfenóis relacionados | Bisfenol E (1,1-bis(4-hidroxifenil)etano) Bisfenol B (2,2-bis(4-hidroxifenil)butano) Bisfenol AP (1,1-bis(4-hidroxifenil)-1-feniletano) Bisfenol C (2,2-bis(3-metil-4-hidroxifenil)propano) Bisfenol S(4,4'-sulfonil-difenol) Bisfenol AF (2,2-bis(4-hidroxifenil)hexafluoropropano) |
| Compostos relacionados | Policarbonato de bisfenol A 2,2-Difenilpropano |
| Página de dados suplementares | |
| Estrutura e propriedades | n, εr, etc. |
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas |
| Dados espectrais | UV, IV, RMN, EM |
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |
Bisfenol A (BPA) é um composto orgânico sintético usado na produção de diversos tipos de plásticos. É solúvel na maioria dos solventes orgânicos, mas pouco solúvel em água.[3] O BPA é produzido em escala industrial através da reação de condensação do fenol com a acetona, e sua produção global está estimada em 10 milhões de toneladas em 2022.[4] A maior aplicação do BPA é como um comonômero na produção de policarbonatos (~65%), seguida pela fabricação de resinas epóxi (~30%).[5][6] O restante é usado principalmente como estabilizante e antioxidante na fabricação de PVC, além de ser matéria-prima em retardantes de chama.[4][6][7]
Os efeitos do BPA na saúde têm sido objeto de prolongado debate público e científico.[8][9][10] O BPA é um xenoestrógeno, isto é, uma substância que interfere no funcionamento do sistema endócrino pois apresenta propriedades semelhantes ao estrogênio.[11] Sendo considerado um disruptor endócrino, o BPA pode provocar efeitos na saúde humana, mesmo em baixas concentrações.[4][12] O composto é encontrado em muitos materiais e produtos comuns,[13] como o revestimento interno de latas de alimentos,[14] produtos têxteis,[15] recibos de compras[16] e brinquedos.[17][18]
Os efeitos do BPA na saúde humana foram estudados por órgãos públicos de saúde em muitos países, assim como pela Organização Mundial da Saúde.[19] Embora os níveis de exposição estejam abaixo do nível de risco atualmente estabelecido pelas agências regulatórias, várias jurisdições tomaram medidas para reduzir a exposição com base no princípio da precaução. Em particular, a proibição do BPA em mamadeiras diminuiu a exposição de bebês ao BPA.[20] Plásticos livres de BPA (BPA-free) feitos com bisfenóis alternativos, como bisfenol S e bisfenol F, foram introduzidos no mercado, mas também há controvérsias sobre seus efeitos na saúde.[21][22]
Desde 2008, países como Estados Unidos e Canadá começaram a restringir o uso de BPA em produtos infantis. Em 2010, alguns países da União Europeia, como Dinamarca, França e Suécia, proibiram o uso de BPA em embalagens alimentares. Desde então, outros países, como China (2011), Japão (2012) e Austrália (2012), também proibiram o seu uso em produtos infantis.[20] No Brasil a ANVISA proibiu a fabricação e importação de mamadeiras que contenham BPA em sua composição em 2011, diminuindo a exposição de lactentes ao composto.[23]
História editar
A síntese do bisfenol A foi descoberta em 1891 pelo químico russo Aleksandr Dianin.[24][25] Em 1934, químicos da da I.G. Farbenindustrie relataram o acoplamento entre o BPA e epicloridrina. Posteriormente, resinas e revestimentos derivados de materiais semelhantes foram descritos por trabalhadores das empresas DeTrey Freres na Suíça e Devoe e Raynolds nos EUA, promovendo o desenvolvimento de resinas epóxi, estimulando a produção de BPA em larga escala.[26] A produção de BPA foi impulsionada ainda mais com o desenvolvimento de plásticos policarbonatos pela Bayer e General Electric. Esses plásticos entraram em circulação em 1958, sendo produzidos pela Mobay, General Electric e Bayer.[27]
O efeito do BPA no sistema endócrino já vinha sendo estudado no início da década de 1930, e o bioquímico britânico Edward Charles Dodds avaliou-o como um estrogênio artificial.[28][29][30] Trabalhos subsequentes determinaram que o BPA se ligava aos receptores de estrogênio dezenas de milhares de vezes mais fracamente do que o estradiol, o principal hormônio sexual feminino.[31][32] Dodds eventualmente desenvolveu um composto estruturalmente semelhante, o dietilestilbestrol (DES), que foi usado como um fármaco estrogênico sintético em mulheres e animais até que foi proibido devido ao seu risco de causar câncer. A proibição do uso de DES em seres humanos veio em 1971 e em animais, em 1979. O BPA nunca foi usado como um fármaco e seus usos se restringiram à fabricação de plásticos.[28]
Em 2003, o consumo anual de BPA nos EUA era de 856 mil toneladas, sendo 72% usados na fabricação de policarbonatos e 21% de resinas epóxi.[33][ligação inativa] Nos Estados Unidos, o BPA é fabricado pela Bayer MaterialScience, Dow Chemical Company, SABIC Innovative Plastics (antes GE Plastics), Hexion Specialty Chemicals e Sunoco Chemicals. Em 2004, essas empresas produziram pouco mais de 1 milhão de toneladas do BPA, em comparação com 7.260 toneladas em 1991.[carece de fontes] Menos de 5% do BPA produzido nos Estados Unidos é utilizado em aplicações de contato com alimentos.[34]
Produção editar
A síntese de Dianin, desenvolvida há mais de 130 anos, ainda é amplamente utilizada na produção do BPA sem grandes alterações. Essa síntese consiste na condensação de dois equivalentes de fenol com acetona (por isso bisfenol A), liberando um equivalente de água (H2O).[35] A reação é catalisada por um ácido forte, como o ácido clorídrico, ácido sulfúrico ou um catalisador sólido ácido.[36] Para garantir a condensação completa e limitar a formação de subprodutos como o composto de Dianin, geralmente é utilizado um grande excesso de fenol. A produção do BPA é relativamente barata devido à grande economia atômica da reação de síntese e à facilidade de obtenção dos materiais de partida através do processo do cumeno.[3] Em 2022, a produção global e foi estimada em 10 milhões de toneladas.[4]
Embora a adição de acetona geralmente ocorra na posição para em ambos os fenóis, no entanto pequenas quantidades de isômeros orto-para e orto-orto também são produzidos, juntamente com vários outros subprodutos.[37] Essas impurezas podem estar presentes em amostras comerciais de BPA.[37][38]
Propriedades editar
O BPA é um composto orgânico que pertence ao grupo dos derivados do difenilmetano. Embora tenha um ponto de fusão alto, ele pode ser facilmente dissolvido em uma ampla gama de solventes como tolueno, etanol e acetato de etila.[39] Para purificar o composto, é possível utilizar a técnica de recristalização em ácido acético com água.[40] Durante a cristalização, os cristais formam-se no grupo espacial monoclínico P 21/n (onde n indica o plano de transflecção), com moléculas individuais de BPA arranjadas em um ângulo de torção de 91,5% entre os anéis de fenol.[41][42][43] Dados espectroscópicos estão disponíveis no AIST.[44]
Usos e aplicações editar
Policarbonatos editar
Cerca de 65-70% de todo o bisfenol A é utilizado para fabricar plásticos policarbonatos,[5][6] cuja massa consiste em quase 90% de BPA. A polimerização é realizada através de uma reação com fosgênio, conduzida sob condições bifásicas; o ácido clorídrico é eliminado com base aquosa.[27] Este processo converte as moléculas individuais de BPA em grandes cadeias poliméricas.
Resinas epóxi e vinil-éster editar
Cerca de 25-30% de todo o BPA é usado na fabricação de resinas epóxi e resinas vinil-éster.[5][6] Para a resina epóxi, é primeiro convertido em éter diglicídico do bisfenol A (geralmente abreviado BADGE ou DGEBA),[45][46] através de uma reação com epicloridrina em meio básico.
O produto (BADGE) ainda pode ser utilizado na fabricação de resinas éster-vinil através da reação com ácido metacrílico para formar bis-GMA. Alternativamente, e em menor grau, o BPA pode ser etoxilado e, em seguida, convertido em seus derivados de diacrilato e dimetacrilato (bis-EMA, ou EBPADMA). Estes produtos podem ser incorporados em baixos níveis em resinas éster-vinil, alterando suas propriedades físicas,[47] para aplicação em resinas dentárias e selantes.[48][49]
Outros usos editar
Os 5% restantes do BPA são usados em uma ampla gama de aplicações, muitas das quais envolvem plástico.[50] BPA é um componente importante de vários plásticos de alto desempenho, a produção destes é baixa em comparação com outros plásticos, mas ainda está na escala de produção de milhares de toneladas por ano. Quantidades comparativamente menores de BPA também são usadas como aditivos ou modificadores em alguns plásticos commodities (tais quais o polietileno, polipropileno, poliestireno e PVC). Esses materiais são comuns, mas o teor de de BPA em sua composição é baixo.
Plásticos: editar
Componente majoritário editar
- Os policianuratos podem ser produzidos a partir do BPA através do seu éster de cianato (BADCy).[50] Este é formado por uma reação entre o BPA e o brometo de cianogênio.[51] Exemplos incluem BT-Epoxy, que é uma das várias resinas usadas na produção de placas de circuito impresso.
- Polieterimidas como Ultem podem ser produzidas a partir de BPA através do deslocamento de um grupo nitro de bisnitroimidas apropriadas.[52][53] Estes plásticos termoplásticos de poli-imidas têm a resistência excepcional a dano mecânico, térmico e químico. Eles são usados em dispositivos médicos e outros instrumentos de alto desempenho.
- As polibenzoaxinas podem ser produzidas a partir de vários fenóis, incluindo o BPA.[54][55]
- As polissulfonas podem ser produzidas a partir de BPA e 4,4’-diclorodifenilsulfona (DCDPS) formando poli(sulfona bisfenol A) (PSF). É usado como uma alternativa de alto desempenho ao policarbonato.[50][56]
- As resinas fenol-formaldeído de bisfenol-A, utilizadas na produção de laminados melamínicos de alta pressão.[50]
Componente minoritário editar
- O BPA pode ser incorporado em espumas de poliuretano seus derivados como extensores de cadeia de segmento duro, particularmente em materiais viscoelásticos.[57][58]
- O PVC pode conter BPA por diversos motivos. O BPA é usado às vezes como um antioxidante em ftalatos,[59] que são extensivamente usados como plastificantes para PVC. O BPA também tem sido usado como um antioxidante para proteger estabilizadores de calor sensíveis usados no PVC. O éter diglicídico do bisfenol A (BADGE) é usado como um sequestrante de ácidos, particularmente em dispersões de PVC, como organosóis ou plastisóis,[60][61] que são usados como revestimentos para o interior de latas de alimentos, bem como estampas de roupas em alto relevo usando técnicas específicas como a serigrafia ou vinil de transferência de calor.[15]
- BPA é usado em retardantes de chama usados em plásticos.[62] A bromação do BPA forma o tetrabromobisfenol A (TBBPA), principalmente usado como um componente reativo de polímeros, o que significa que é incorporado na cadeia principal do polímero. É usado para preparar policarbonatos resistentes ao fogo, substituindo certa quantidade de bisfenol A. TBBPA de menor qualidade está presente em resinas epóxi usadas em placas de circuito impresso. O TBBPA também é convertido em tetrabromobisfenol A-bis(2,3- dibromopropil éter) (TBBPA-BDBPE) que pode ser usado como retardante de chama em polipropileno. O TBBPA-BDBPE não é ligado quimicamente ao polímero e pode ser lixiviado, isto é, migrar para o ambiente.[63] O uso desses compostos está diminuindo devido às restrições aos retardantes de chama bromados. A reação do BPA com cloreto de fosforila e fenol forma o difosfato de bisfenol A (BADP), que é usado como retardador de chama líquido em algumas misturas poliméricas de alto desempenho, como misturas de policarbonato/ABS.[64]
Outras Aplicações editar
- BPA é usado como um antioxidante em fluidos de freio.[65]
- BPA é usado como um agente de desenvolvimento em papel térmico (recibos de loja).[16]
- Os produtos de papel reciclado também podem conter BPA,[66] embora isso possa depender de como é reciclado. A remoção da tinta (deinking) pode eliminar 95% do BPA, porém se esse processo não for realizado, o BPA permanece nas fibras, e o papel é geralmente reciclado em papelão ondulado.[5]
- O BPA etoxilado encontra menor uso como 'agente nivelador' na galvanoplastia.
- Derivados do BPA estão sendo investigados como fármacos, como o EPI-001 e seus derivados.[67]
Produtos que podem conter BPA no Brasil editar
Este artigo ou seção pode conter informações desatualizadas. (Março de 2015) |
No Brasil, os fabricantes são obrigados por lei a informarem "ostensiva e adequadamente, a presença de Bisfenol A (BPA) nas embalagens e rótulos de produtos que contenham essa substância em sua composição" desde o início de 2011.[68]
Por precaução, a importação e fabricação de mamadeiras que contenham Bisfenol A está proibida desde janeiro de 2012 conforme a Resolução RDC n.41/2011.[68] No entanto, para outros produtos de plástico "o BPA ainda é permitido, mas a legislação estabelece limite máximo de migração específica desta substância para o alimento que foi definido com base nos resultados de estudos toxicológicos."
Produtos livres de BPA (BPA-free) podem conter outros tipos de bisfenol que, assim como o BPA, podem apresentar efeitos nocivos à saúde mediante a exposição.[21][22]
Substitutos do Bisfenol A editar
Preocupações com os efeitos do BPA na saúde levaram alguns fabricantes a substituí-lo por outros bisfenóis, como o bisfenol S e o bisfenol F. Estes compostos são produzidos de maneira semelhante ao BPA, substituindo a acetona por outras cetonas, que sofrem reações de condensação análogas.[3] Preocupações de saúde também foram levantadas sobre esses substitutos.[22][69]
| Fórmula estrutural | Nome | CAS | Reagentes | |
|---|---|---|---|---|
| Bisfenol AF | 1478-61-1 | Fenol | Hexafluoroacetona | |
| Bisfenol F | 620-92-8 | Fenol | Formaldeído | |
| Bisfenol S | 80-09-1 | Fenol | Trióxido de enxofre | |
| Bisfenol Z | 843-55-0 | Fenol | Ciclohexanona | |
| Tetrametil bisfenol F | 5384-21-4 | 2,6-xilenol | Formaldeído | |
Efeitos sobre a saúde editar
Este artigo ou seção pode conter informações desatualizadas. (Março de 2015) |
Os efeitos do Bisfenol A (BPA) na saúde têm sido objeto de um longo debate público e científico,[8][9][10] com a PubMed listando mais de 16.000 artigos científicos até 2022.[70] Estudos iniciais na década de 1930 mostraram que o BPA afeta o sistema endócrino e foi avaliado como um estrogênio artificial pelo bioquímico britânico Edward Charles Dodds.[11][28][29][30] O BPA foi identificado como uma substância de alta prioridade para a avaliação de risco à saúde humana.[71] Um estudo da Food and Drug Administration (FDA) de 2010 levantou preocupações quanto à exposição de fetos, bebês e crianças pequenas ao BPA.[72] De acordo com o Greenpeace, é uma substância com graves riscos para a saúde.[73]
A maior parte dos estudos está relacionada à atividade do BPA como um desregulador do sistema endócrino, embora possa interagir com outros sistemas receptores,[74] causando danos ao fígado, interrupção da função pancreática de células-β, perturbações hormonais na tireoide e promoção da obesidade.[71] Essas interações são consideradas fracas, mas a exposição ao BPA é efetiva ao longo da vida, levando à preocupação com efeitos potencialmente cumulativos.[8] Estudar este tipo de interação com baixas doses e a longo prazo é difícil e, embora tenham havido estudos numerosos, existem discrepâncias consideráveis em suas conclusões a respeito dos efeitos observados assim como dos níveis em que ocorrem.[8]
Uma crítica comum é que os testes financiados pela indústria tendem a mostrar o BPA como sendo mais seguro do que os estudos realizados por laboratórios acadêmicos ou governamentais,[10][75] embora isso também tenha sido explicado em termos de estudos financiados pela indústria sendo melhor projetados.[9][76] Os autores que alegam a superioridade dos estudos financiados pela indústria estão vinculados a órgãos regulatórios e/ou empresas químico-farmacêuticas.[9][76]
Embora o BPA apresente toxicidade aguda muito baixa, como indicado pela sua DL50 de 4 g/kg (em ratos). os relatórios indicam que ele é um irritante menor para a pele, embora menos do que o fenol.[3] Em 2015, com base em dados de um estudo de toxicidade reprodutiva multigeracional em ratos, foi estabelecida uma ingestão diária tolerável temporária (t-TDI) de 4 µg/kg de peso corporal por dia foi estabelecida pelo Painel da Autoridade Europeia para a Segurança Alimentar (EFSA) sobre Materiais de Contato com Alimentos, Enzimas Aromatizantes e Auxiliares de Processamento. Com base na incerteza científica e nos resultados de um estudo do Programa Nacional de Toxicologia (NTP),[77] a EFSA está atualmente reavaliando este t-TDI.[17]
Exposição editar
Devido à presença do BPA em plásticos e outros materiais comuns, a maioria das pessoas é frequentemente exposta a vestígios do composto.[78][79][80] A principal fonte de exposição humana é através de alimentos, uma vez que epóxi e PVC são usados para revestir o interior de latas de alimentos para evitar a corrosão do metal. Os recipientes de bebidas de policarbonato também são uma fonte de exposição relevante, embora a maioria das garrafas de bebidas descartáveis seja feita de PET, que não contém BPA. Entre as fontes não alimentares, as rotas de exposição incluem poeira,[6] papel térmico,[16] roupas,[15] materiais odontológicos[81] e dispositivos médicos.[13]
Embora a exposição ao BPA seja comum, sua acumulação no corpo é pequena, uma vez que estudos toxicocinéticos mostram que a meia-vida biológica do BPA em humanos adultos é de cerca de duas horas.[82][83] Após a exposição e absorção, o corpo converte o BPA em compostos mais solúveis em água via glucuronidação ou sulfatação. Então, esses derivados são removidos do corpo através da urina. Isso permite que a exposição seja facilmente determinada por testes de urina, facilitando o biomonitoramento do composto em populações.[13][20][84]
Farmacologia editar
Descobriu-se que o BPA interage com uma gama diversificada de receptores hormonais, tanto em humanos quanto em animais.[74] O composto se liga a ambos os receptores nucleares de estrogênio (ERs), ERα e ERβ. O BPA pode apresentar tanto um efeito semelhante ao estrogênio, quanto assumir um papel de antagonista do hormônio, indicando que é ou um modulador seletivo do receptor do estrogênio (SERM), ou um agonista parcial do ER. Apesar disso, ele é de 1000 a 2000 vezes menos potente que o estradiol, o principal hormônio sexual feminino em humanos.[85]
Em altas concentrações o BPA também se liga como um antagonista ao receptor de andrógenos (RA). Além da ligação ao receptor, verificou-se que o composto afeta a esteroidogênese de celulas de Leydig, incluindo a expressão de 17α-hidroxilase/17,20 liase e aromatase, e interfere na interação receptor-ligante do hormônio luteinizante (LH).[85]
O bisfenol A interage com o receptor gama relacionado ao estrogênio (ERR-γ). Este receptor órfão (sem ligante endógeno conhecido) se comporta como um ativador constitutivo da transcrição. BPA parece se ligar fortemente a ERR-γ (constante de dissociação = 5,5 nm), mas apenas fracamente ao RE. A ligação do BPA ao ERR-γ preserva a sua atividade constitutiva basal. O composto pode igualmente protegê-lo da desativação do SERM 4-hydroxitamoxifeno (afimoxifeno). Esse pode ser o mecanismo pelo qual o BPA atua como xenoestrogênio.[86] A distribuição da expressão de ERR-γ em diferentes partes do corpo pode ser responsável pelas variações do efeito do bisfenol A. Verificou-se também que o BPA atua como agonista do receptor de estrogênio acoplado à proteína G (GPER/GPR30).[87]
Disruptor endócrino editar
O bisfenol A é um disruptor endócrino que pode estar relacionado a patogênese de várias doenças.[88][89][90][91][92] Em 2009 a Endocrine Society divulgou comunicado científico expressando preocupação com a exposição humana corrente ao BPA.[92] Nesta revisão da literatura, os autores argumentam que disruptores endócrinos (incluindo o BPA) apresentam efeitos tanto no sistema reprodutor feminino quanto no sistema reprodutor masculino.[92]
De acordo com o relatório de 2008 do Programa Nacional de Toxicologia (NTP) dos EUA, a atual exposição humana ao BPA é de "alguma preocupação" para efeitos no desenvolvimento da próstata e cérebro e para efeitos comportamentais em fetos, bebês e crianças.[93] Mais recentemente, a Agência Europeia dos Produtos Químicos (ECHA) identificou o BPA como uma "substância de grande preocupação" devido às suas propriedades de reprotoxicidade e desregulação endócrina.[17]
Síndrome do Ovário Policístico editar
Os efeitos do Bisfenol como disruptor endócrino podem estar relacionados à patogênese da síndrome do ovário policístico (SOP). Esses efeitos potencialmente são transferidos de maneira epigenética para as filhas de mães que foram expostas ao BPA.[94]
O BPA parece desregular a produção do hormônio liberador de gonadotropinas (GnRH) - note-se que ao nível da glândula pituitária (hipófise), produtos químicos industriais (incluindo-se o BPA), por si só, foram capazes de perturbar a liberação de gonadotrofinas.[95] Consequentemente, tais distúrbios, conforme se viu acima em Causas relacionadas a desordens endócrinas, encontram-se na raiz da Síndrome do Ovário Policístico - SOP, até mesmo porque a produção exarcebada do hormônio liberador de gonadotropinas (GnRH) desequilibra a produção do Hormônio luteinizante (LH) em proporção superior à do Hormônio Folículo Estimulante (FSH).[95] Este aumento do Hormônio luteinizante (LH) seria o estimulador da superprodução de andrógenos, fato que se agrega à produção exagerada de androgênios pelos ovários.[96]
Gestantes expostas ao BPA podem apresentar um desequilíbrio hormonal que pode aumentar as chances de que o feto, no caso de ser do sexo feminino, desenvolva a síndrome do ovário policístico (SOP).[94] Além disso, observa-se que mulheres adultas já diagnosticadas com SOP podem sofrer um agravamento da sintomatologia típica da síndrome acaso entrem em contato com disruptores endócrinos como o BPA.[carece de fontes]
Funcionamento da tireóide editar
Estudo de 2007 concluiu que o BPA bloqueia os receptores do hormônio da tireóide.[97]
Sistema reprodutor e comportamento sexual editar
Estudos de 2009 apontam para anomalias do ovário e efeitos carcinogênicos por exposição durante períodos pré-natais críticos de diferenciação, alteração permanente dos mecanismos hipotalâmicos estrógeno-dependentes que organizam o comportamento sexual da fêmea de ratos exposta no período neonatal, disfunção sexual masculina referida por adultos que trabalham com BPA.[98]
Pesquisa realizada em 2010 demonstrou que o BPA aumenta o risco de disfunções sexuais masculinas, reduz a concentração e qualidade do sêmen, segundo estudo publicado na revista “Fertility and Sterility”. A pesquisa foi realizada durante cinco anos com 514 operários que trabalhavam em fábricas da China.[99]
Outros efeitos editar
Em 2007 um painel do National Institutes of Health, nos EUA, demonstrou "alguma preocupação" sobre o efeito do BPA sobre o desenvolvimento cerebral e comportamento de fetos e bebês.[100] Estudo com primatas da Yale School of Medicine observou interferência do BPA em conexões celulares do cérebro vitais para a memória, aprendizagem e humor.[101][102] Hiperatividade, déficit de atenção e aumento da sensibilidade a drogas de abuso resultam do aumento da atividade mesolímbica da dopamina potencialmente causada pelo mimetismo da atividade estrogênica pelo BPA.[103]
Estudo de 2008 concluiu que a exposição neonatal ao BPA pode afetar o comportamento ligado ao dimorfismo sexual no adulto. Também em 2008 conclui-se que o BPA afeta, mesmo em nanodosagem, o processo da memória, porque altera a potenciação a longo prazo do hipocampo.[carece de fontes]
O BPA é considerado tóxico para o fígado e os rins (após exposição prolongada) e tem uma classificação harmonizada na União Europeia (UE) como tóxico para a reprodução.[17]
Estudo de 2009 baseado em experimentos com ser humanos e dados epidemiológicos reforça a hipótese de que a exposição fetal ao composto seja uma das causas subjacentes do aumento do câncer de mama nos últimos 50 anos.[104]
Estudo in vitro de 2007 mostrou aumento permanente de tamanho da próstata com concentrações de BPA usualmente encontradas no soro humano.[105]
Toxicologia editar
Toxicocinética editar
O BPA é absorvido e metabolizado de forma diferente em humanos e roedores.[106][107] Em humanos, uma dose única é rapidamente excretada pela urina após a completa metabolização hepática do BPA para o glucuronídeo de BPA,[108][109][110] enquanto o sulfato do BPA é um metabólito minoritário.[111] Em roedores, o BPA sofre recirculação entero-hepática, o que resulta em uma clearance mais lenta e um tempo de meia-vida mais longo do BPA livre.[106] O BPA livre é o composto tóxico, e a capacidade de conjugação é importante na avaliação do risco.[112][113][114] Fetos e recém-nascidos podem ser mais sensíveis ao BPA devido à sua incapacidade de glucuronidar o BPA de forma eficaz e à redução da depuração.[115]
Toxicidade editar
Estudos epidemiológicos mostraram associações estatisticamente significativas entre a exposição ao BPA e doenças coronárias, distúrbios reprodutivos e alterações comportamentais em jovens do sexo feminino. No entanto, de acordo com o painel da EFSA estudos transversais não permitem estabelecer relações causais.[116] Estudos in vitro e in vivo demonstraram mecanismos endócrinos potencialmente relevantes mediados pelo BPA, mas não há um modo de ação claramente definido para o BPA em baixas doses. Não é possível avaliar a relevância toxicológica dos efeitos do BPA descritos, e eles não podem ser considerados na derivação da ingestão diária aceitável. O Painel da EFSA não considerou este efeito adverso reprodutível.[116]
Doses elevadas de BPA, acima de 5 mg/kg de peso corporal por dia, podem ter efeitos semelhantes aos observados com outras substâncias estrogênicas. Alguns efeitos também foram relatados em exposições a baixas doses de BPA, que podem não estar relacionados com os receptores hormonais clássicos. O BPA tem uma afinidade fraca por esses receptores, mas pode ter efeitos por meio de outras vias de sinalização. No entanto, devido à falta de evidências claras e falhas no desenho dos experimentos, não é possível concluir se as alterações bioquímicas e moleculares observadas têm impacto na saúde humana. Não se pode avaliar a relevância toxicológica dos efeitos do BPA em baixas doses, e os resultados não podem ser usados para definir a ingestão diária aceitável. Embora alguns estudos sugiram efeitos adversos reprodutíveis do BPA em doses baixas, a EFSA não considera esses efeitos como consistentes.[116]
Efeitos ambientais editar
Este artigo ou seção pode conter informações desatualizadas. (Março de 2015) |
Distribuição e degradação editar
O BPA tem sido detectado no meio ambiente natural desde a década de 1990, e agora já está amplamente distribuído pelo globo.[117][118] É um poluente principalmente de águas doces superficiais,[119] mas também tem sido encontrado no ambiente marinho,[120] nos solos[121] e, em níveis mais baixos, na atmosfera. A solubilidade do BPA na água é baixa (~ 300 g/ tonelada de água),[122] no entanto, isso já possibilita a distribuição do composto no meio ambiente.[121] Boa parte da poluição por BPA acontece através da água, particularmente através das águas residuais de indústrias que utilizam BPA. A reciclagem de papel, quando inclui o papel térmico,[5] pode ser uma importante fonte de liberação do composto no meio ambiente. A lixiviação do BPA em materiais de PVC[119] e de aterros sanitários[123] também podem ser fontes significativas.
Em todos esses casos, o tratamento de águas residuais pode ser altamente eficaz na remoção de BPA, reduzindo em até 91-98% a concentração do composto.[124] Independente disso, os 2-9% restantes continuarão a ser liberados no meio ambiente, sendo que baixos níveis de BPA comumente observados em águas superficiais e sedimentos nos EUA e na Europa.[125]
Uma vez no meio ambiente, o BPA é biodegradado através de processos aeróbicos por uma grande variedade de organismos.[117][126][127] Sua meia-vida em água foi estimada entre 4,5 e 15 dias.[121] A degradação no ar é mais rápida do que na água, enquanto no solo é mais lenta.[121] O BPA em sedimentos degrada-se ainda mais lentamente, particularmente onde este processo é anaeróbico. A degradação abiótica já foi reportada, mas geralmente é mais lenta que a biodegradação. Os mecanismos de degradação abiótica incluem a foto-oxidação e reações com minerais, tais como o goethita, que podem estar presente no solo ou em sedimentos.[128]
Impactos à vida selvagem editar
O BPA é um contaminante emergente preocupante.[123] Apesar de não apresentar uma elevada bioacumulação e sua meia-vida ser curta, a liberação do BPA no ambiente expõe continuamente a plantas[129] e animais ao composto. Embora muitos estudos tenham sido realizados, estes geralmente se concentram em uma gama limitada de organismos modelo e podem usar concentrações de BPA muito maiores que os níveis comumente encontrados no meio ambiente.[130] Dessa forma, os efeitos precisos do BPA no crescimento, reprodução e desenvolvimento do organismo aquático não são totalmente compreendidos.[130] Independentemente disso, os dados existentes mostram que os efeitos do BPA na vida selvagem geralmente são negativos.[131][132] O BPA parece ser capaz de afetar o desenvolvimento e a reprodução em uma ampla gama de animais selvagens,[132] com certas espécies sendo particularmente sensíveis, como invertebrados e anfíbios.[131]
Regulação do uso de BPA editar
Este artigo ou seção pode conter informações desatualizadas. (Março de 2015) |
O bisfenol A é uma substância proibida em vários países, incluindo Canadá, Dinamarca e Costa Rica, além de alguns estados norte-americanos. No Brasil, o BPA era utilizado na produção de garrafas plásticas, mamadeiras, copos para bebês e vários outros produtos de plástico.[133] Em 2011, a fabricação de mamadeiras com BPA foi proibida no país, e projetos de lei visando a proibição parcial da substância em produtos voltados para o público infantil estavam em tramitação no Congresso Nacional.[134][135][136]
Outros países também têm adotado medidas para restringir o uso do BPA. Em 2011, a Comissão Europeia proibiu a produção, venda e importação de mamadeiras com BPA para a União Europeia, e a China propôs a proibição do BPA em qualquer tipo de recipiente concebido para conter alimentos ou bebidas para crianças.[137][138][139]
Embora órgãos reguladores como a FDA (EUA) e a ANVISA (Brasil) tenham determinado níveis seguros para seres humanos, novos estudos científicos têm levantado questionamentos e revisões sobre esses níveis. Os anos iniciais do desenvolvimento humano parecem ser o período de maior sensibilidade aos efeitos do BPA. Em 2011, um estudo conduzido pelo Comitê de Aconselhamento da Sociedade Alemã de Toxicologia concluiu que, de acordo com os dados atualmente disponíveis, a exposição ao BPA não representa riscos para a saúde humana, incluindo recém-nascidos e bebês.[140][141][142]
Recomendações aos pais editar
De acordo com artigo publicado na Veja a recomendação para os pais é que "Se puder, substitua mamadeiras, copos, pratos e recipientes para guardar alimentos de plástico por aqueles que que sejam feitos de vidro, madeira, porcelana, aço ou metal. Ao comprar qualquer produto, especialmente para crianças, busque informações nos rótulos das embalagens, como o selo bisfenol free, os números 3 e 7 no símbolo da reciclagem ou uma certificação de órgãos como o Inmetro e a Anvisa. Não compre brinquedos ou qualquer tipo de produto que sejam de má qualidade, principalmente para crianças pequenas. Se tiver em casa utensílios de cozinha de plástico, evite colocá-los no microondas ou mesmo congelar alimentos nesses recipientes. Produtos de plástico velhos, danificados ou vencidos devem ser jogados no lixo".[143]
Estudos relevantes editar
Um estudo prospectivo de coorte foi realizado para avaliar o impacto das exposições ao BPA durante a gestação e a infância no comportamento e na função executiva em crianças de 3 anos de idade, e se o gênero da criança modifica essas associações. O estudo constatou que a exposição ao BPA durante a gestação afetou os domínios comportamentais e de regulação emocional, especialmente em meninas. Porém, as associações entre exposição ao BPA na infância e neurocomportamento foram em grande parte nulas e não modificadas pelo gênero da criança. Os clínicos podem aconselhar os pacientes preocupados a reduzir a exposição a certos produtos de consumo, mas os benefícios dessas reduções são incertos.[144]
Um estudo semelhante examinou se a exposição neonatal ao BPA pode afetar a expressão dos receptores de estrogênio β (ERβ) em áreas específicas do cérebro em ratos, o que pode levar a mudanças no comportamento sociosexual em animais adultos. Os resultados indicaram que a exposição ao BPA durante os primeiros dias de vida resultou em mudanças na expressão do ERβ em áreas do cérebro críticas para o comportamento sociosexual, sendo que tais mudanças foram específicas de acordo com a região do cérebro e o sexo. Além disso, a exposição ao estradiol benzoato também causou redução na expressão do ERβ em áreas cerebrais femininas e masculinas. Esses resultados sugerem que a exposição ao BPA e outros disruptores endócrinos durante o período neonatal pode afetar o desenvolvimento sexual do cérebro e ter implicações no comportamento sociosexual em animais adultos.[145]
No artigo A ameaça dos disruptores endócrinos, de José Santamarta, o autor resgata aspectos centrais das pesquisas já realizadas para alertar a todos nós que estamos sendo vítimas de certas substâncias químicas que, por diferentes mecanismos, estão afetando especialmente os processos reprodutivos de aves e mamíferos. Tais substâncias, agindo no sistema endócrino, inclusive dos seres humanos, podem colocar em risco nossa sobrevivência como espécie. Os chamados disruptores endócrinos (ou burladores, fraudadores) não são venenos clássicos, eles interferem no sistema hormonal, sabotando as comunicações e alterando os mensageiros químicos que se movem, permanentemente, dentro do nosso corpo. Como resultado, estamos sujeitos a um conjunto de efeitos maléficos à saúde, o que inclui anormalidades sexuais em crianças e adultos, homens e mulheres. Nos homens, pesquisas mostram a redução drástica do número de espermatozoides no sêmen.[146][ligação inativa]
Um artigo de revisão descreve abordagens atuais e novas para os mecanismos patogênicos da SOP e o papel potencial do bisfenol A como disruptor endócrino. Observações sugerem níveis mais elevados de BPA em fluidos biológicos de mulheres com SOP e seu papel na patogênese do hiperandrogenismo e da hiperglicemia. Parece que a exposição da mãe ao BPA durante a gravidez também pode levar ao desenvolvimento de SOP na prole feminina.[94]
Outra revisão constata que estudos mostraram uma correlação positiva entre BPA e andrógenos, sendo que mulheres com SOP apresentam níveis mais elevados de testosterona do que mulheres saudáveis, o que pode levar a um aumento dos níveis de BPA. Por outro lado, o BPA pode aumentar diretamente os níveis de testosterona por meio de duas vias potenciais: inibindo a atividade de duas hidroxilases diferentes da testosterona, levando a uma diminuição do catabolismo da testosterona e consequentemente um aumento da sua concentração, ou atuando como um ligante potente da globulina de ligação aos hormônios sexuais no fígado, deslocando os andrógenos dos sítios de ligação da globulina e aumentando a concentração de andrógenos livres circulantes. Além disso, o BPA está fortemente associado à resistência à insulina, o que pode levar ao desenvolvimento de diabetes tipo 2 em mulheres com SOP.[95]
Referências
- ↑ a b c Registo de Bisphenol A na Base de Dados de Substâncias GESTIS do IFA, accessado em 19 de Novembro de 2007
- ↑ Thieme Chemistry (Hrsg.): Römpp Online. Version 3.1. Georg Thieme Verlag, Stuttgart 2007.
- ↑ a b c d Ullmann's encyclopedia of industrial chemistry. Phenol Derivatives 6ª ed. ed. Weinheim, Alemanha: Wiley‐VCH. 2000. ISBN 9783527306732. OCLC 751968805
- ↑ a b c d Abraham, Anna; Chakraborty, Paromita (1 de junho de 2020). «A review on sources and health impacts of bisphenol A». Reviews on Environmental Health (em inglês) (2): 201–210. ISSN 2191-0308. doi:10.1515/reveh-2019-0034. Consultado em 14 de dezembro de 2022
- ↑ a b c d e Institute for Health Consumer Protection, European Commission Joint Research Centre (2010). «Updated European Union risk assessment report : 4,4'-isopropylidenediphenol (bisphenol-A) : environment addendum of February 2008». op.europa.eu (em inglês). doi:10.2788/40195. Consultado em 17 de dezembro de 2022
- ↑ a b c d e Vasiljevic, Tijana; Harner, Tom (1 de outubro de 2021). «Bisphenol A and its analogues in outdoor and indoor air: Properties, sources and global levels». Science of The Total Environment (em inglês). 148013 páginas. ISSN 0048-9697. doi:10.1016/j.scitotenv.2021.148013. Consultado em 14 de dezembro de 2022
- ↑ Síntese, caracterização e aplicação de polímeros conjugados derivados de ferroceno e de bisfenol-A. Gonçalves, Camila dos Santos. Tese de Doutorado no Instituto de Química da Universidade de São Paulo
- ↑ a b c d World Health Organization; Nations, Food and Agriculture Organization of the United (2011). «Joint FAO/WHO expert meeting to review toxicological and health aspects of bisphenol A : final report, including report of stakeholder meeting on bisphenol A, 1-5 November 2010, Ottawa, Canada» (em inglês). Consultado em 19 de dezembro de 2022
- ↑ a b c d Hengstler, J. G.; Foth, H.; Gebel, T.; Kramer, P.-J.; Lilienblum, W.; Schweinfurth, H.; Völkel, W.; Wollin, K.-M.; Gundert-Remy, U. (abril de 2011). «Critical evaluation of key evidence on the human health hazards of exposure to bisphenol A». Critical Reviews in Toxicology (em inglês) (4): 263–291. ISSN 1040-8444. doi:10.3109/10408444.2011.558487. Consultado em 14 de dezembro de 2022
- ↑ a b c Myers, John Peterson; vom Saal, Frederick S.; Akingbemi, Benson T.; Arizono, Koji; Belcher, Scott; Colborn, Theo; Chahoud, Ibrahim; Crain, D. Andrew; Farabollini, Francesca (março de 2009). «Why Public Health Agencies Cannot Depend on Good Laboratory Practices as a Criterion for Selecting Data: The Case of Bisphenol A». Environmental Health Perspectives (3): 309–315. ISSN 0091-6765. PMC 2661896 . PMID 19337501. doi:10.1289/ehp.0800173. Consultado em 14 de dezembro de 2022
- ↑ a b Goloubkova, Tatiana; Spritzer, Poli Mara (agosto de 2000). «Xenoestrogênios: o exemplo do bisfenol-A». Arquivos Brasileiros de Endocrinologia & Metabologia: 323–330. ISSN 1677-9487. doi:10.1590/S0004-27302000000400008. Consultado em 14 de dezembro de 2022
- ↑ Almeida, Susana; Raposo, António; Almeida-González, Maira; Carrascosa, Conrado (novembro de 2018). «Bisphenol A: Food Exposure and Impact on Human Health: Bisphenol A and human health effect…». Comprehensive Reviews in Food Science and Food Safety (em inglês) (6): 1503–1517. doi:10.1111/1541-4337.12388. Consultado em 14 de dezembro de 2022
- ↑ a b c Geens, Tinne; Aerts, Dominique; Berthot, Carl; Bourguignon, Jean-Pierre; Goeyens, Leo; Lecomte, Philippe; Maghuin-Rogister, Guy; Pironnet, Anne-Madeleine; Pussemier, Luc (1 de outubro de 2012). «A review of dietary and non-dietary exposure to bisphenol-A». Food and Chemical Toxicology (em inglês) (10): 3725–3740. ISSN 0278-6915. doi:10.1016/j.fct.2012.07.059. Consultado em 18 de dezembro de 2022
- ↑ Noonan, Gregory O.; Ackerman, Luke K.; Begley, Timothy H. (13 de julho de 2011). «Concentration of Bisphenol A in Highly Consumed Canned Foods on the U.S. Market». Journal of Agricultural and Food Chemistry (em inglês) (13): 7178–7185. ISSN 0021-8561. doi:10.1021/jf201076f. Consultado em 17 de dezembro de 2022
- ↑ a b c Xue, Jingchuan; Liu, Wenbin; Kannan, Kurunthachalam (2 de maio de 2017). «Bisphenols, Benzophenones, and Bisphenol A Diglycidyl Ethers in Textiles and Infant Clothing». Environmental Science & Technology (em inglês) (9): 5279–5286. ISSN 0013-936X. doi:10.1021/acs.est.7b00701. Consultado em 17 de dezembro de 2022
- ↑ a b c Björnsdotter, Maria K.; de Boer, Jacob; Ballesteros-Gómez, Ana (1 de setembro de 2017). «Bisphenol A and replacements in thermal paper: A review». Chemosphere (em inglês): 691–706. ISSN 0045-6535. doi:10.1016/j.chemosphere.2017.05.070. Consultado em 17 de dezembro de 2022
- ↑ a b c d den Braver-Sewradj, Shalenie P.; van Spronsen, Rob; Hessel, Ellen V. S. (7 de fevereiro de 2020). «Substitution of bisphenol A: a review of the carcinogenicity, reproductive toxicity, and endocrine disruption potential of alternative substances». Critical Reviews in Toxicology (em inglês) (2): 128–147. ISSN 1040-8444. doi:10.1080/10408444.2019.1701986. Consultado em 14 de dezembro de 2022
- ↑ Xiao, Changyun; Wang, Lihong; Zhou, Qing; Huang, Xiaohua (15 de fevereiro de 2020). «Hazards of bisphenol A (BPA) exposure: A systematic review of plant toxicology studies». Journal of Hazardous Materials (em inglês). 121488 páginas. ISSN 0304-3894. doi:10.1016/j.jhazmat.2019.121488. Consultado em 14 de dezembro de 2022
- ↑ OMS (2010). Toxicological and health aspects of Bisphenol A : report of Joint FAO/WHO Expert Meeting 2-5 November 2010 and report of Stakeholder Meeting on Bisphenol A. Ottawa, Canadá: World Health Organization. OCLC 759446793
- ↑ a b c Huang, Ri-ping; Liu, Ze-hua; Yin, Hua; Dang, Zhi; Wu, Ping-xiao; Zhu, Neng-wu; Lin, Zhang (1 de junho de 2018). «Bisphenol A concentrations in human urine, human intakes across six continents, and annual trends of average intakes in adult and child populations worldwide: A thorough literature review». Science of The Total Environment (em inglês): 971–981. ISSN 0048-9697. doi:10.1016/j.scitotenv.2018.01.144. Consultado em 14 de dezembro de 2022
- ↑ a b Thoene, Michael; Dzika, Ewa; Gonkowski, Slawomir; Wojtkiewicz, Joanna (fevereiro de 2020). «Bisphenol S in Food Causes Hormonal and Obesogenic Effects Comparable to or Worse than Bisphenol A: A Literature Review». Nutrients (em inglês) (2). 532 páginas. ISSN 2072-6643. doi:10.3390/nu12020532. Consultado em 14 de dezembro de 2022
- ↑ a b c Chen, Da; Kannan, Kurunthachalam; Tan, Hongli; Zheng, Zhengui; Feng, Yong-Lai; Wu, Yan; Widelka, Margaret (7 de junho de 2016). «Bisphenol Analogues Other Than BPA: Environmental Occurrence, Human Exposure, and Toxicity—A Review». Environmental Science & Technology (em inglês) (11): 5438–5453. ISSN 0013-936X. doi:10.1021/acs.est.5b05387. Consultado em 14 de dezembro de 2022
- ↑ Bernardo, Paulo Eduardo Masselli; Navas, Sandra Aparecida; Murata, Lúcia Tieco Fukushima; Alcântara, Maria Rosa da Silva de (2015). «Bisfenol A: o uso em embalagens para alimentos, exposição e toxicidade - Uma Revisão» (PDF). Rev. Inst. Adolfo Lutz: 1–11. Consultado em 14 de dezembro de 2022
- ↑ «Organische Chemie». Berichte der deutschen chemischen Gesellschaft (em alemão) (3): 314–337. Janeiro de 1892. ISSN 0365-9496. doi:10.1002/cber.18920250333. Consultado em 15 de dezembro de 2022
- ↑ Zincke, Theodor (1905). «Ueber die Einwirkung von Brom und von Chlor auf Phenole: Substitutionsprodukte, Pseudobromide und Pseudochloride». Justus Liebigs Annalen der Chemie. 343: 75–99. doi:10.1002/jlac.19053430106
- ↑ Pham, Ha Q.; Marks, Maurice J. (15 de outubro de 2005). Wiley-VCH Verlag GmbH & Co. KGaA, ed. «Epoxy Resins». Weinheim, Germany: Wiley-VCH Verlag GmbH & Co. KGaA (em inglês): a09_547.pub2. ISBN 978-3-527-30673-2. doi:10.1002/14356007.a09_547.pub2. Consultado em 15 de dezembro de 2022
- ↑ a b Serini, Volker (15 de junho de 2000). Wiley-VCH Verlag GmbH & Co. KGaA, ed. «Polycarbonates». Weinheim, Germany: Wiley-VCH Verlag GmbH & Co. KGaA (em inglês): a21_207. ISBN 978-3-527-30673-2. doi:10.1002/14356007.a21_207. Consultado em 15 de dezembro de 2022
- ↑ a b c Vogel, Sarah A. (1 de novembro de 2009). «The Politics of Plastics: The Making and Unmaking of Bisphenol A "Safety"». American Journal of Public Health (S3): S559–S566. ISSN 0090-0036. doi:10.2105/AJPH.2008.159228. Consultado em 15 de dezembro de 2022
- ↑ a b Dodds, E. C.; Lawson, Wilfrid (junho de 1936). «Synthetic strogenic Agents without the Phenanthrene Nucleus». Nature (em inglês) (3476): 996–996. ISSN 1476-4687. doi:10.1038/137996a0. Consultado em 15 de dezembro de 2022
- ↑ a b Dodds, Edward Charles; Lawson, W.; Dale, Henry Hallett (27 de abril de 1938). «Molecular structure in relation to oestrogenic activity. Compounds without a phenanthrene nucleus». Proceedings of the Royal Society of London. Series B - Biological Sciences (839): 222–232. doi:10.1098/rspb.1938.0023. Consultado em 15 de dezembro de 2022
- ↑ Kwon, Jung-Hwan; Katz, Lynn E.; Liljestrand, Howard M. (1 de outubro de 2007). «Modeling binding equilibrium in a competitive estrogen receptor binding assay». Chemosphere (em inglês) (7): 1025–1031. ISSN 0045-6535. doi:10.1016/j.chemosphere.2007.04.047. Consultado em 15 de dezembro de 2022
- ↑ Blair, Robert M.; Fang, Hong; et. al (1 de março de 2000). «The Estrogen Receptor Relative Binding Affinities of 188 Natural and Xenochemicals: Structural Diversity of Ligands». Toxicological Sciences. 54: 138–153
- ↑ National Toxicology Program, U.S. Department of Health and Human Services (26 de novembro de 2007). «CERHR Expert Panel Report for Bisphenol A» (PDF). Consultado em 18 de abril de 2008
- ↑ «Bisphenol A Action Plan» (PDF). U.S. Environmental Protection Agency. 29 de março de 2010. Consultado em 12 de Abril de 2010
- ↑ Uglea, Constantin V. (1991). Synthesis and characterization of oligomers. Ioan I. Negulescu. Boca Raton, Fla.: CRC Press. OCLC 22767118
- ↑ de Angelis, A.; Ingallina, P.; Perego, C. (28 de janeiro de 2004). «Solid Acid Catalysts for Industrial Condensations of Ketones and Aldehydes with Aromatics». Industrial & Engineering Chemistry Research (5): 1169–1178. ISSN 0888-5885. doi:10.1021/ie030429+. Consultado em 16 de dezembro de 2022
- ↑ a b Terasaki, Masanori; Nomachi, Makoto; Edmonds, John S; Morita, Masatoshi (1 de maio de 2004). «Impurities in industrial grade 4,4′-isopropylidene diphenol (bisphenol A): possible implications for estrogenic activity». Chemosphere (em inglês) (6): 927–931. ISSN 0045-6535. doi:10.1016/j.chemosphere.2003.11.063. Consultado em 16 de dezembro de 2022
- ↑ Pahigian, Jamie M.; Zuo, Yuegang (1 de setembro de 2018). «Occurrence, endocrine-related bioeffects and fate of bisphenol A chemical degradation intermediates and impurities: A review». Chemosphere (em inglês): 469–480. ISSN 0045-6535. doi:10.1016/j.chemosphere.2018.05.117. Consultado em 16 de dezembro de 2022
- ↑ Haynes, William M. (22 de junho de 2016). CRC Handbook of Chemistry and Physics (em inglês). [S.l.]: CRC Press
- ↑ Perrin, Douglas Dalzell; Armarego, W. L. F. (1988). Purification of Laboratory Chemicals (em inglês). [S.l.]: Butterworth-Heinemann
- ↑ ccdc. «2,2-bis(4-Hydroxyphenyl)propane». www.ccdc.cam.ac.uk. Consultado em 16 de dezembro de 2022
- ↑ Okada, Kenji (15 de julho de 1996). «X-ray crystal structure analyses and atomic charges of color former and developer. I. Color developers». Journal of Molecular Structure (em inglês) (3): 223–233. ISSN 0022-2860. doi:10.1016/0022-2860(95)09168-8. Consultado em 16 de dezembro de 2022
- ↑ Wolak, J. E.; Knutson, J.; Martin, J. D.; Boyle, P.; Sargent, Andrew L.; White, Jeffery L. (6 de novembro de 2003). «Dynamic Disorder and Conformer Exchange in the Crystalline Monomer of Polycarbonate». The Journal of Physical Chemistry B (48): 13293–13299. ISSN 1520-6106. doi:10.1021/jp036527q. Consultado em 16 de dezembro de 2022
- ↑ SDBS. «SDBS-1716 (4,4'-isopropylidenediphenol)». sdbs.db.aist.go.jp. Consultado em 16 de dezembro de 2022
- ↑ Ng, Feifei; Couture, Guillaume; Philippe, Coralie; Boutevin, Bernard; Caillol, Sylvain (janeiro de 2017). «Bio-Based Aromatic Epoxy Monomers for Thermoset Materials». Molecules (em inglês) (1). 149 páginas. ISSN 1420-3049. doi:10.3390/molecules22010149. Consultado em 17 de dezembro de 2022
- ↑ Encyclopedia of chemical technology vol.5. Raymond E. Kirk, Donald F. Othmer, Jacqueline I. Kroschwitz, Mary Howe-Grant. New York: [s.n.] 1998. OCLC 23650978
- ↑ Gonçalves, Flávia; Kawano, Yoshio; Pfeifer, Carmem; Stansbury, Jeffrey W.; Braga, Roberto R. (agosto de 2009). «Influence of BisGMA, TEGDMA, and BisEMA contents on viscosity, conversion, and flexural strength of experimental resins and composites». European Journal of Oral Sciences (em inglês) (4): 442–446. doi:10.1111/j.1600-0722.2009.00636.x. Consultado em 17 de dezembro de 2022
- ↑ Sideridou, I.; Tserki, V.; Papanastasiou, G. (1 de abril de 2002). «Effect of chemical structure on degree of conversion in light-cured dimethacrylate-based dental resins». Biomaterials (em inglês) (8): 1819–1829. ISSN 0142-9612. doi:10.1016/S0142-9612(01)00308-8. Consultado em 17 de dezembro de 2022
- ↑ Sideridou, Irini D.; Achilias, Dimitris S. (julho de 2005). «Elution study of unreacted Bis-GMA, TEGDMA, UDMA, and Bis-EMA from light-cured dental resins and resin composites using HPLC». Journal of Biomedical Materials Research Part B: Applied Biomaterials (em inglês) (1): 617–626. ISSN 1552-4973. doi:10.1002/jbm.b.30252. Consultado em 17 de dezembro de 2022
- ↑ a b c d Geens, Tinne; Goeyens, Leo; Covaci, Adrian (1 de setembro de 2011). «Are potential sources for human exposure to bisphenol-A overlooked?». International Journal of Hygiene and Environmental Health (em inglês) (5): 339–347. ISSN 1438-4639. doi:10.1016/j.ijheh.2011.04.005. Consultado em 17 de dezembro de 2022
- ↑ Chemistry and technology of cyanate ester resins. Ian Hamerton 1st ed ed. London: Blackie Academic & Professional. 1994. OCLC 31608371
- ↑ Takekoshi, T.; Kochanowski, J. E.; Manello, J. S.; Webber, M. J. (junho de 1985). «Polyetherimides. I. Preparation of dianhydrides containing aromatic ether groups». Journal of Polymer Science: Polymer Chemistry Edition (6): 1759–1769. doi:10.1002/pol.1985.170230616. Consultado em 17 de dezembro de 2022
- ↑ Handbook of thermoset plastics. Sidney H. Goodman, Dodiuk Hanna 3rd ed ed. San Diego: William Andrew. 2014. OCLC 864742805
- ↑ Vijayakumar, C.T.; Shamim Rishwana, S.; Surender, R.; David Mathan, N.; Vinayagamoorthi, S.; Alam, S. (2 de janeiro de 2014). «Structurally diverse benzoxazines: synthesis, polymerization, and thermal stability». Designed Monomers and Polymers (em inglês) (1): 47–57. ISSN 1568-5551. doi:10.1080/15685551.2013.797216. Consultado em 17 de dezembro de 2022
- ↑ Ghosh, N. N.; Kiskan, B.; Yagci, Y. (1 de novembro de 2007). «Polybenzoxazines—New high performance thermosetting resins: Synthesis and properties». Progress in Polymer Science (em inglês) (11): 1344–1391. ISSN 0079-6700. doi:10.1016/j.progpolymsci.2007.07.002. Consultado em 17 de dezembro de 2022
- ↑ John Wiley & Sons, Inc, ed. (4 de dezembro de 2000). Kirk‐Othmer Encyclopedia of Chemical Technology (em inglês) 1 ed. [S.l.]: Wiley
- ↑ Laza, José Manuel; Veloso, Antonio; Vilas, José Luis (10 de janeiro de 2021). «Tailoring new bisphenol a ethoxylated shape memory polyurethanes». Journal of Applied Polymer Science (em inglês) (2). 49660 páginas. ISSN 0021-8995. doi:10.1002/app.49660. Consultado em 17 de dezembro de 2022
- ↑ Król, Piotr (2008). Linear polyurethanes : synthesis methods, chemical structures, properties and applications. Leiden: VSP. OCLC 244205505
- ↑ JRC (16 de julho de 2008). «European Union Summary Risk Assessment Report - Bis (2-ethylhexyl) Phthalate (DEHP)». JRC Publications Repository (em inglês). Consultado em 17 de dezembro de 2022
- ↑ Shah, Ashok C.; Poledna, David J. (setembro de 2003). «Review of PVC dispersion and blending resin products». Journal of Vinyl and Additive Technology (em inglês) (3): 146–154. ISSN 1083-5601. doi:10.1002/vnl.10076. Consultado em 17 de dezembro de 2022
- ↑ Shah, Ashok C.; Poledna, David J. (setembro de 2002). «Review of specialty PVC resins». Journal of Vinyl and Additive Technology (em inglês) (3): 214–221. ISSN 1083-5601. doi:10.1002/vnl.10365. Consultado em 17 de dezembro de 2022
- ↑ Dagani, Michael J.; Barda, Henry J.; Benya, Theodore J.; Sanders, David C. (15 de junho de 2000). Wiley-VCH Verlag GmbH & Co. KGaA, ed. «Bromine Compounds». Weinheim, Germany: Wiley-VCH Verlag GmbH & Co. KGaA (em inglês): a04_405. ISBN 978-3-527-30673-2. doi:10.1002/14356007.a04_405. Consultado em 17 de dezembro de 2022
- ↑ Gauthier, Lewis T.; Laurich, Bruce; Hebert, Craig E.; Drake, Christine; Letcher, Robert J. (20 de agosto de 2019). «Tetrabromobisphenol-A-Bis(dibromopropyl ether) Flame Retardant in Eggs, Regurgitates, and Feces of Herring Gulls from Multiple North American Great Lakes Locations». Environmental Science & Technology (em inglês) (16): 9564–9571. ISSN 0013-936X. doi:10.1021/acs.est.9b02472. Consultado em 17 de dezembro de 2022
- ↑ Pawlowski, Kristin H; Schartel, Bernhard (novembro de 2007). «Flame retardancy mechanisms of triphenyl phosphate, resorcinol bis(diphenyl phosphate) and bisphenol A bis(diphenyl phosphate) in polycarbonate/acrylonitrile–butadiene–styrene blends». Polymer International (em inglês) (11): 1404–1414. doi:10.1002/pi.2290. Consultado em 17 de dezembro de 2022
- ↑ Lamprea, Katerine; Bressy, Adèle; Mirande-Bret, Cécile; Caupos, Emilie; Gromaire, Marie-Christine (1 de agosto de 2018). «Alkylphenol and bisphenol A contamination of urban runoff: an evaluation of the emission potentials of various construction materials and automotive supplies». Environmental Science and Pollution Research (em inglês) (22): 21887–21900. ISSN 1614-7499. doi:10.1007/s11356-018-2272-z. Consultado em 17 de dezembro de 2022
- ↑ Liao, Chunyang; Kannan, Kurunthachalam (1 de novembro de 2011). «Widespread Occurrence of Bisphenol A in Paper and Paper Products: Implications for Human Exposure». Environmental Science & Technology (em inglês) (21): 9372–9379. ISSN 0013-936X. doi:10.1021/es202507f. Consultado em 17 de dezembro de 2022
- ↑ Agarwal, N.; Lorenzo, G. Di; Sonpavde, G.; Bellmunt, J. (1 de setembro de 2014). «New agents for prostate cancer». Annals of Oncology (em inglês) (9): 1700–1709. ISSN 0923-7534. PMID 24658665. doi:10.1093/annonc/mdu038. Consultado em 17 de dezembro de 2022
- ↑ a b «Bisfenol A». Agência Nacional de Vigilância Sanitária - Anvisa. Consultado em 17 de dezembro de 2022
- ↑ Rochester, Johanna R.; Bolden, Ashley L. (1 de julho de 2015). «Bisphenol S and F: A Systematic Review and Comparison of the Hormonal Activity of Bisphenol A Substitutes». Environmental Health Perspectives (7): 643–650. PMC 492270 . PMID 25775505. doi:10.1289/ehp.1408989. Consultado em 18 de dezembro de 2022
- ↑ «bisphenol a - Search Results - pmcacessodata=2022-12-19». pmclingua=en
- ↑ a b Le Corre, L.; Besnard, P.; Chagnon, M.-C. (12 de maio de 2015). «BPA, an Energy Balance Disruptor». Critical Reviews in Food Science and Nutrition (em inglês) (6): 769–777. ISSN 1040-8398. doi:10.1080/10408398.2012.678421. Consultado em 19 de dezembro de 2022
- ↑ «Update on Bisphenol A for Use in Food Contact Applications: January 2010». U.S. Food and Drug Administration. 15 de janeiro de 2010. Consultado em 15 de Janeiro de 2010
- ↑ «Bisphenol A Action Plan». Greenpeace Espanha. 27 de dezembro de 2010. Consultado em 29 de dezembro de 2010
- ↑ a b MacKay, Harry; Abizaid, Alfonso (1 de maio de 2018). «A plurality of molecular targets: The receptor ecosystem for bisphenol-A (BPA)». Hormones and Behavior. Endocrine Disrupting Chemicals and Behavior (em inglês): 59–67. ISSN 0018-506X. doi:10.1016/j.yhbeh.2017.11.001. Consultado em 19 de dezembro de 2022
- ↑ vom, Saal Frederick S.; Hughes, Claude (1 de agosto de 2005). «An Extensive New Literature Concerning Low-Dose Effects of Bisphenol A Shows the Need for a New Risk Assessment». Environmental Health Perspectives (8): 926–933. PMC 1280330 . PMID 16079060. doi:10.1289/ehp.7713. Consultado em 19 de dezembro de 2022
- ↑ a b Teeguarden, Justin G.; Hanson-Drury, Sesha (1 de dezembro de 2013). «A systematic review of Bisphenol A "low dose" studies in the context of human exposure: A case for establishing standards for reporting "low-dose" effects of chemicals». Food and Chemical Toxicology (em inglês): 935–948. ISSN 0278-6915. doi:10.1016/j.fct.2013.07.007. Consultado em 19 de dezembro de 2022
- ↑ «Abstract for RR-09». ntp.niehs.nih.gov (em inglês). Consultado em 28 de dezembro de 2022
- ↑ Calafat, Antonia M.; Ye, Xiaoyun; Wong, Lee-Yang; Reidy, John A.; Needham, Larry L. (1 de janeiro de 2008). «Exposure of the U.S. Population to Bisphenol A and 4-tertiary-Octylphenol: 2003–2004». Environmental Health Perspectives (1): 39–44. PMC 2199288 . PMID 18197297. doi:10.1289/ehp.10753. Consultado em 18 de dezembro de 2022
- ↑ Thoene, M; Nowicka, N; Wojtkiewicz, J (26 de abril de 2018). «The state of bisphenol research in the lesser developed countries of the EU: a mini-review». Toxicology Research (em inglês). 7 (3): 371–380. doi:10.1039/c8tx00064f
- ↑ Vandenberg, Laura N.; Hauser, Russ; Marcus, Michele; Olea, Nicolas; Welshons, Wade V. (1 de agosto de 2007). «Human exposure to bisphenol A (BPA)». Reproductive Toxicology (em inglês) (2): 139–177. ISSN 0890-6238. doi:10.1016/j.reprotox.2007.07.010. Consultado em 18 de dezembro de 2022
- ↑ Van Landuyt, K. L.; Nawrot, Tim; Geebelen, B.; De Munck, J.; Snauwaert, J.; Yoshihara, K.; Scheers, Hans; Godderis, Lode; Hoet, P. (1 de agosto de 2011). «How much do resin-based dental materials release? A meta-analytical approach». Dental Materials (em inglês) (8): 723–747. ISSN 0109-5641. doi:10.1016/j.dental.2011.05.001. Consultado em 18 de dezembro de 2022
- ↑ Tsukioka, Tadashi; Terasawa, Jun-ichi; Sato, Shouichiro; Hatayama, Yoshiyuki; Makino, Tsunehisa; Nakazawa, Hiroyuki (2004). «Development of Analytical Method for Determining Trace Amounts of BPA in Urine Samples and Estimation of Exposure to BPA». Journal of Environmental Chemistry (1): 57–63. doi:10.5985/jec.14.57. Consultado em 18 de dezembro de 2022
- ↑ Shin, Beom Soo; Kim, Chul Hwan; Jun, Yoon Sik; Kim, Dong Hwan; Lee, Byung Mu; Yoon, Chi Ho; Park, Eun Hye; Lee, Kang Choon; Han, Soon-Young (dezembro de 2004). «PHYSIOLOGICALLY BASED PHARMACOKINETICS OF BISPHENOL A». Journal of Toxicology and Environmental Health, Part A (em inglês) (23-24): 1971–1985. ISSN 1528-7394. doi:10.1080/15287390490514615. Consultado em 18 de dezembro de 2022
- ↑ Bousoumah, Radia; Leso, Veruscka; Iavicoli, Ivo; Huuskonen, Pasi; Viegas, Susana; Porras, Simo P.; Santonen, Tiina; Frery, Nadine; Robert, Alain (20 de agosto de 2021). «Biomonitoring of occupational exposure to bisphenol A, bisphenol S and bisphenol F: A systematic review». Science of The Total Environment (em inglês). 146905 páginas. ISSN 0048-9697. doi:10.1016/j.scitotenv.2021.146905. Consultado em 18 de dezembro de 2022
- ↑ a b Akingbemi, Benson T.; Sottas, Chantal M.; Koulova, Anna I.; Klinefelter, Gary R.; Hardy, Matthew P. (1 de fevereiro de 2004). «Inhibition of Testicular Steroidogenesis by the Xenoestrogen Bisphenol A Is Associated with Reduced Pituitary Luteinizing Hormone Secretion and Decreased Steroidogenic Enzyme Gene Expression in Rat Leydig Cells». Endocrinology (2): 592–603. ISSN 0013-7227. doi:10.1210/en.2003-1174. Consultado em 19 de dezembro de 2022
- ↑ Matsushima, A.; Kakuta, Y.; Teramoto, T.; Koshiba, T.; Liu, X.; Okada, H.; Tokunaga, T.; Kawabata, S.-i.; Kimura, M. (25 de julho de 2007). «Structural Evidence for Endocrine Disruptor Bisphenol A Binding to Human Nuclear Receptor ERR». Journal of Biochemistry (4): 517–524. ISSN 0021-924X. doi:10.1093/jb/mvm158. Consultado em 19 de dezembro de 2022
- ↑ Prossnitz, Eric R.; Barton, Matthias (25 de maio de 2014). «Estrogen biology: New insights into GPER function and clinical opportunities». Molecular and Cellular Endocrinology. Beneficial Effect of Estrogens in the Brain and Cardiovascular System and Estrogen Effects in Brain and Heart (em inglês) (1): 71–83. ISSN 0303-7207. PMC 4040308 . PMID 24530924. doi:10.1016/j.mce.2014.02.002. Consultado em 19 de dezembro de 2022
- ↑ Gore, Andrea C. (8 de junho de 2007). Endocrine-Disrupting Chemicals: From Basic Research to Clinical Practice (em inglês). [S.l.]: Springer Science & Business Media
- ↑ O’Connor, JC; Chapin, RE (2003). «Critical evaluation of observed adverse effects of endocrine active substances on reproduction and development, the immune system, and the nervous system» (Full Article). Pure Appl. Chem. 75 (11–12): 2099–2123. doi:10.1351/pac200375112099. Consultado em 28 de fevereiro de 2007
- ↑ Okada H, Tokunaga T, Liu X, Takayanagi S, Matsushima A, Shimohigashi Y (2008). «Direct evidence revealing structural elements essential for the high binding ability of bisphenol A to human estrogen-related receptor-gamma». Environ. Health Perspect. 116 (1): 32–8. PMC 2199305 . PMID 18197296. doi:10.1289/ehp.10587
- ↑ vom Saal FS, Myers JP (2008). «Bisphenol A and Risk of Metabolic Disorders». Journal of the American Medical Association (JAMA). 300 (300). 1353 páginas. PMID 18799451. doi:10.1001/jama.300.11.1353
- ↑ a b c Diamanti-Kandarakis, Evanthia; Bourguignon, Jean-Pierre; Giudice, Linda C.; Hauser, Russ; Prins, Gail S.; Soto, Ana M.; Zoeller, R. Thomas; Gore, Andrea C. (junho de 2009). «Endocrine-disrupting chemicals: an Endocrine Society scientific statement». Endocrine Reviews (4): 293–342. ISSN 1945-7189. PMC 2726844 . PMID 19502515. doi:10.1210/er.2009-0002. Consultado em 28 de dezembro de 2022
- ↑ «NTP Finalizes Report on Bisphenol A». National Institutes of Health (NIH) (em inglês). 28 de setembro de 2015. Consultado em 28 de dezembro de 2022
- ↑ a b c Rutkowska, Aleksandra; Rachoń, Dominik (1 de abril de 2014). «Bisphenol A (BPA) and its potential role in the pathogenesis of the polycystic ovary syndrome (PCOS)». Gynecological Endocrinology (4): 260–265. ISSN 0951-3590. PMID 24397396. doi:10.3109/09513590.2013.871517. Consultado em 10 de março de 2023
- ↑ a b c Industrial endocrine disruptors and polycystic ovary syndrome. Palioura E, Diamanti-Kandarakis E. J Endocrinol Invest. 2013 Dec;36(11):1105-11 (http://www.ncbi.nlm.nih.gov/pubmed/24445124)
- ↑ Lab Tests On-line. Ovário Policístico (http://www.labtestsonline.org.br/understanding/conditions/pcos/). Este artigo foi modificado pela última vez em 4 de fevereiro de 2013.
- ↑ Zoeller, R. (2007). "Environmental chemicals impacting the thyroid: targets and consequences". Thyroid : official journal of the American Thyroid Association 17 (9): 811–817.
- ↑ http://dx.doi.org/10.1093/humrep/dep381
- ↑ Metro Brasil de 29 de outubro de 2010 página 18
- ↑ NTP-CERHR EXPERT PANEL REPORT on the REPRODUCTIVE and DEVELOPMENTAL TOXICITY of BISPHENOL A
- ↑ Leranth C, Hajszan T, Szigeti-Buck K, Bober J, Maclusky NJ (2008). «Bisphenol A prevents the synaptogenic response to estradiol in hippocampus and prefrontal cortex of ovariectomized nonhuman primates». Proc. Natl. Acad. Sci. U.S.A. 105 (37). 14187 páginas. PMC 2544599 . PMID 18768812. doi:10.1073/pnas.0806139105
- ↑ Layton, Lindsey (4 de setembro de 2008). «Chemical in Plastic Is Connected to Health Problems in Monkeys». Washington Post. pp. A02. Consultado em 6 de setembro de 2008
- ↑ Suzuki; Mizuo, K; Miyagawa, K; Narita, M (2005). "Exposure to bisphenol-A affects the rewarding system in mice". Nihon shinkei seishin yakurigaku zasshi = Japanese journal of psychopharmacology 25 (3): 125–8.
- ↑ Brisken, C. (2008). "Endocrine Disruptors and Breast Cancer". CHIMIA International Journal for Chemistry 62: 406–409.
- ↑ Prins, G. (2008). "Developmental exposure to bisphenol a increases prostate cancer susceptibility in adult rats: epigenetic mode of action is implicated". Fertility and Sterility 89: e41-e41.
- ↑ a b EFSA (European Food Safety Authority). Opinion of the Scientific Panel on Food Additives, Flavourings, Processing Aids and Materials in Contact with Food on a request from the Commission related to 2,2-bis(4-hydroxyphenyl)propane (Bisphenol A). The EFSA Journal 2006; 428: 1-75.
- ↑ EFSA (European Food Safety Authority). Scientific Opinion of the Panel on Food additives, Flavourings, Processing aids and Materials in Contact with Food (AFC) on a request from the Commission on the toxicokinetics of Bisphenol A. The EFSA Journal 2008a; 759: 1-10.
- ↑ Völkel W, Kiranoglu M, Fromme H. Determination of free and total bisphenol A in human urine to assess daily uptake as a basis for a valid risk assessment. Toxicol Lett 2008; 179: 15562.
- ↑ Völkel W, Colnot T, Csanady GA, Filser JG, Dekant W. Metabolism and kinetics of bisphenol a in humans at low doses following oral administration. Chem Res Toxicol 2002; 15: 1281-7.
- ↑ Tsukioka T, Terasawa J, Sato S, Hatayama Y, Makino T, Nakazawa H. Development of analytical method for determining trace amounts of BPA in urine samples and estimation of exposure to BPA. J Environ Chem 2004; 14: 5763.
- ↑ Ye X, Kuklenyik Z, Needham LL, Calafat AM. Quantification of urinary conjugates of bisphenol A, 2,5-dichlorophenol, and 2-hydroxy-4-methoxybenzophenone in humans by online solid phase extraction-high performance liquid chromatography-tandem mass spectrometry. Anal Bioanal Chem 2005; 383: 638-44.
- ↑ Snyder RW, Maness SC, Gaido KW, Welsch F, Sumner SC, Fennell TR. Metabolism and disposition of bisphenol A in female rats. Toxicology and Applied Pharmacology 2000; 168: 225-34.
- ↑ Shimizu M, Ohta K, Matsumoto Y, Fukuoka M, Ohno Y, Ozawa S. Sulphation of bisphenol A abolished its estrogenicity based on proliferation and gene expression in human breast cancer MCF-7 cells. Toxicol In vitro 2002; 16: 549-56.
- ↑ Willhite CC, Ball GL, McLellan CJ. Derivation of a bisphenol A oral reference dose (RfD) and drinking-water equivalent concentration. Journal of Toxicology and Environmental Health B Critical Reviews 2008; 11: 69-146.
- ↑ «Screening Assessment for The Challenge (Bisphenol A)». 2008
- ↑ a b c EFSA (European Food Safety Authority). Scientific Opinion on Bisphenol A: evaluation of a study investigating its neurodevelopmental toxicity, review of recent scientific literature on its toxicity and advice on the Danish risk assessment of Bisphenol A. The EFSA Journal 2010; 8 (9): 1829.
- ↑ a b Staples, Charles A.; Dome, Philip B.; Klecka, Gary M.; Oblock, Sondra T.; Harris, Lynne R. (1 de abril de 1998). «A review of the environmental fate, effects, and exposures of bisphenol A». Chemosphere (em inglês) (10): 2149–2173. ISSN 0045-6535. doi:10.1016/S0045-6535(97)10133-3. Consultado em 20 de dezembro de 2022
- ↑ Occurrence of phthalates and bisphenol A and F in the environment. Hermann Fromme; Thomas Küchlerb, Thomas Ottoc, Konstanze Pilzc, Josef Müllerb, Andrea Wenzelb. Water Research. Volume 36, Issue 6, March 2002, Pages 1429–1438
- ↑ a b Corrales, Jone; Kristofco, Lauren A.; Steele, W. Baylor; Yates, Brian S.; Breed, Christopher S.; Williams, E. Spencer; Brooks, Bryan W. (1 de julho de 2015). «Global Assessment of Bisphenol A in the Environment: Review and Analysis of Its Occurrence and Bioaccumulation». Dose-Response (em inglês) (3). 155932581559830 páginas. ISSN 1559-3258. PMC 4674187 . PMID 26674671. doi:10.1177/1559325815598308. Consultado em 20 de dezembro de 2022
- ↑ Ozhan, Koray; Kocaman, Emel (1 de fevereiro de 2019). «Temporal and Spatial Distributions of Bisphenol A in Marine and Freshwaters in Turkey». Archives of Environmental Contamination and Toxicology (em inglês) (2): 246–254. ISSN 1432-0703. doi:10.1007/s00244-018-00594-6. Consultado em 20 de dezembro de 2022
- ↑ a b c d Cousins, I.T.; Staples, C.A.; Kleĉka, G.M.; Mackay, D. (1 de julho de 2002). «A Multimedia Assessment of the Environmental Fate of Bisphenol A». Human and Ecological Risk Assessment: An International Journal (5): 1107–1135. ISSN 1080-7039. doi:10.1080/1080-700291905846. Consultado em 20 de dezembro de 2022
- ↑ Shareef, Ali; Angove, Michael J.; Wells, John D.; Johnson, Bruce B. (11 de maio de 2006). «Aqueous Solubilities of Estrone, 17β-Estradiol, 17α-Ethynylestradiol, and Bisphenol A». Journal of Chemical & Engineering Data (em inglês) (3): 879–881. ISSN 0021-9568. doi:10.1021/je050318c. Consultado em 20 de dezembro de 2022
- ↑ a b Qi, Chengdu; Huang, Jun; Wang, Bin; Deng, Shubo; Wang, Yujue; Yu, Gang (1 de janeiro de 2018). «Contaminants of emerging concern in landfill leachate in China: A review». Emerging Contaminants (em inglês) (1): 1–10. ISSN 2405-6650. doi:10.1016/j.emcon.2018.06.001. Consultado em 20 de dezembro de 2022
- ↑ Drewes, Jörg E.; Hemming, Jocelyn; Ladenburger, Sarah J.; Schauer, James; Sonzogni, William (janeiro de 2005). «An Assessment of Endocrine Disrupting Activity Changes during Wastewater Treatment through the Use of Bioassays and Chemical Measurements». Water Environment Research (em inglês) (1): 12–23. doi:10.2175/106143005X41573. Consultado em 20 de dezembro de 2022
- ↑ Klečka, Gary M.; Staples, Charles A.; Clark, Kathryn E.; van der Hoeven, Nelly; Thomas, David E.; Hentges, Steven G. (15 de agosto de 2009). «Exposure Analysis of Bisphenol A in Surface Water Systems in North America and Europe». Environmental Science & Technology (em inglês) (16): 6145–6150. ISSN 0013-936X. doi:10.1021/es900598e. Consultado em 20 de dezembro de 2022
- ↑ Kang, Jeong-Hun; Katayama, Yoshiki; Kondo, Fusao (16 de janeiro de 2006). «Biodegradation or metabolism of bisphenol A: From microorganisms to mammals». Toxicology (em inglês) (2): 81–90. ISSN 0300-483X. doi:10.1016/j.tox.2005.10.001. Consultado em 20 de dezembro de 2022
- ↑ Zhang, Chi; Li, Yi; Wang, Chao; Niu, Lihua; Cai, Wei (2 de janeiro de 2016). «Occurrence of endocrine disrupting compounds in aqueous environment and their bacterial degradation: A review». Critical Reviews in Environmental Science and Technology (1): 1–59. ISSN 1064-3389. doi:10.1080/10643389.2015.1061881. Consultado em 20 de dezembro de 2022
- ↑ Im, Jeongdae; Löffler, Frank E. (16 de agosto de 2016). «Fate of Bisphenol A in Terrestrial and Aquatic Environments». Environmental Science & Technology (em inglês) (16): 8403–8416. ISSN 0013-936X. doi:10.1021/acs.est.6b00877. Consultado em 20 de dezembro de 2022
- ↑ Xiao, Changyun; Wang, Lihong; Zhou, Qing; Huang, Xiaohua (15 de fevereiro de 2020). «Hazards of bisphenol A (BPA) exposure: A systematic review of plant toxicology studies». Journal of Hazardous Materials (em inglês). 121488 páginas. ISSN 0304-3894. doi:10.1016/j.jhazmat.2019.121488. Consultado em 20 de dezembro de 2022
- ↑ a b Rubin, Alexander M.; Seebacher, Frank (1 de julho de 2022). «Bisphenols impact hormone levels in animals: A meta-analysis». Science of The Total Environment (em inglês). 154533 páginas. ISSN 0048-9697. doi:10.1016/j.scitotenv.2022.154533. Consultado em 20 de dezembro de 2022
- ↑ a b Wu, Nicholas C.; Seebacher, Frank (julho de 2020). «Effect of the plastic pollutant bisphenol A on the biology of aquatic organisms: A meta‐analysis». Global Change Biology (em inglês) (7): 3821–3833. ISSN 1354-1013. doi:10.1111/gcb.15127. Consultado em 20 de dezembro de 2022
- ↑ a b Oehlmann, Jörg; Schulte-Oehlmann, Ulrike; Kloas, Werner; Jagnytsch, Oana; Lutz, Ilka; Kusk, Kresten O.; Wollenberger, Leah; Santos, Eduarda M.; Paull, Gregory C. (27 de julho de 2009). «A critical analysis of the biological impacts of plasticizers on wildlife». Philosophical Transactions of the Royal Society B: Biological Sciences (1526): 2047–2062. PMC 2873012 . PMID 19528055. doi:10.1098/rstb.2008.0242. Consultado em 20 de dezembro de 2022
- ↑ Folha: Ministério instaura inquérito para apurar risco de composto de plástico à saúde
- ↑ Mamadeiras com bisfenol serão banidas até final de 2011. Revista Exame, 19 de setembro de 2011.
- ↑ O QUE É BISFENOL A? (http://www.otaodoconsumo.com.br/bisfenol/)
- ↑ http://www1.folha.uol.com.br/equilibrioesaude/937199-piracicaba-e-primeira-cidade-do-brasil-a-proibir-o-bisfenol-a.shtml
- ↑ http://eur-lex.europa.eu/LexUriServ/LexUriServ.do?uri=OJ:L:2011:026:0011:0014:EN:PDF
- ↑ http://www.shanghaidaily.com/nsp/National/2011/03/05/China%2Bto%2Bban%2Bplastic%2Bbottles%2Bto%2Bfeed%2Bbabies/
- ↑ Byrne, Jane (22 de setembro de 2008). «Consumers fear the packaging - a BPA alternative is needed now». Consultado em 5 de janeiro de 2010
- ↑ http://informahealthcare.com/doi/abs/10.3109/10408444.2011.558487
- ↑ Draft Screening Assessment for The Challenge Phenol, 4,4' -(1-methylethylidene)bis- (Bisphenol A)Chemical Abstracts Service Registry Number 80-05-7. Health Canada, 2008.
- ↑ Ginsberg G, Rice DC (2009). «Does Rapid Metabolism Ensure Negligible Risk from Bisphenol A?». EPH. 117 (11): 1639–1643. doi:10.1289/ehp.0901010
- ↑ «Como manter o bisfenol A longe de seu filho». VEJA. Consultado em 13 de dezembro de 2022
- ↑ Impact of early-life bisphenol A exposure on behavior and executive function in children. Braun JM, Kalkbrenner AE, Calafat AM, Yolton K, Ye X, Dietrich KN, Lanphear BP. Pediatrics. 2011 Nov;128(5):873-82. doi: 10.1542/peds.2011-1335. Epub 2011 Oct 24 (http://www.ncbi.nlm.nih.gov/pubmed/22025598).
- ↑ Sex Specific Estrogen Receptor beta (ERβ) mRNA Expression in the Rat Hypothalamus and Amygdala is Altered by Neonatal Bisphenol A (BPA) Exposure. Jinyan Cao, Linwood Joyner, Jillian A. Mickens, Stephanie M Leyrer and Heather B Patisaul. Reproduction. 2014; 147(4): 537–554. Published online Mar 4, 2014. doi: 10.1530/REP-13-0501 (http://www.ncbi.nlm.nih.gov/pmc/articles/PMC3947720/).
- ↑ A ameaça dos disruptores endócrinos. José Santamarta; traduzido por Francisco Roberto Caporal. Agroecologia e Desenvolvimento Rural Sustentável, Porto Alegre, v.2, n.3, jul./set.2001: 18-29 (ISSN 1519-1060) Revista da EMATER/RS.
Ligações externas editar
- Bisfenol A - Generalidades e Aspectos Toxicológicos
- Dinamarca e França proíbem o uso do bisfenol A em produtos infantis
- Canadá proíbe o uso de policarbonato na fabricação de mamadeiras, SBQ
- Bisfenol A passa da placenta para o feto - Crescer
- How to Protect Your Baby from BPA (Bisphenol A)
- Plastic Not Fantastic with Bisphenol A - Scientific American
- US FDA statement on bisphenol A from 2008
- Myers, John Peterson; et al. (março de 2009). «Why Public Health Agencies Cannot Depend on Good Laboratory Practices as a Criterion for Selecting Data: The Case of Bisphenol A». Environmental Health Perspectives. 17 (3): 309–315
- Hazard in a bottle Attempt to regulate BPA in California defeated (from The Economist)
- Bisphenol-A News & Products News commentary on BPA Containing Products
- Layton, Lyndsey (23 de fevereiro de 2010). «Alternatives to BPA containers not easy for U.S. foodmakers to find». Washington Post. Consultado em 23 de fevereiro de 2010
- «Piracicaba é primeira cidade do Brasil a proibir o bisfenol-A». Folha.com. 30 de junho de 2011
- Superinteressante, Disruptores endócrinos nos plásticos: como isso prejudica a sua vida?, 05/02/2013;
- EMBALAGENS PLÁSTICAS NA BERLINDA. Conheça efeitos do bisfenol-a, encontrado em copos, garrafas e mais
- Bisfenol A – Hormônio Sintético na Dieta
- O GLOBO: Conheça alguns dos segredos da indústria de alimentos, guardados a sete-chaves, e revelados aqui.
- Sociedade Brasileira de Endocrinologia e Metabologia: CBAEM/COPEM: Os Perigos do Bisfenol;
- Sociedade Brasileira de Endocrinologia e Metabologia: Desreguladores endócrinos: eles estão dentro e fora das nossas casas.
- Revista Veja: Estudo revela novos danos causados pelo bisfenol A. Em roedores, a substância afetou o comportamento sexual dos animais.
- Bisfenol A pode afetar comportamento de meninas. Gestantes que são expostas à substância do plástico têm filhas mais ansiosas;
- Agência de Notícias Reuters: BPA tied to behavior problems in girls (em português: Bisfenol - BPA - ligado a problemas de comportamento em garotas).
- Agência de Notícias do Estado de São Paulo: Bisfenol A está ligado a problemas de comportamento em garotas, diz estudo.
- Agência de Notícias do Estado de São Paulo: Estudo revela novos danos causados pelo Bisfenol A;
- "Dental Composites for Kids: Even Worse Than Mercury Amalgam?" (em português: "Compósitos odontológicos para Crianças: ainda piores do que os de Amálgama de Mercúrio?");
- "Don't Put Your Coffee in Plastic Cups" (em português: "Não coloque o seu café em copos de plástico");
- "10 Steps to Remove BPA from Your Body in Less Than a Week" (em português: "10 passos para remover o BPA do seu corpo em menos de 01 semana");
- "Why 'BPA-Free' Plastics Aren't Safe" (em português: "Por que o 'BPA-Free não é seguro'") ;
- Unimed: você sabia que o café quente em contato com o copo plástico pode liberar toxinas cancerígenas?
- Não Coloque Seu Café em Copo Plástico;
