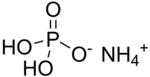
Di-hidrogenofosfato de amônio
As referências deste artigo necessitam de formatação. (Setembro de 2021) |
Dihidrogenofosfato de amônio, ou fosfato de monoamônio, ou ainda fosfato monoamônico, citado às vezes como ADP, do inglês ammonium dihydrogen phosphate, composto químico de fórmula NH4H2PO4, é formado quando uma solução de ácido fosfórico é adicionado à amônia até a solução estar distintamente ácida. Cristaliza-se em prismas tetragonais. Fosfato de monoamônio é frequentemente usado na composição de fertilizantes agrícolas secos. Ele supre o solo com os elementos nitrogênio e fósforo numa forma que é usável pelas plantas. O composto é também um componente do pó ABC em alguns extintores de incêndio de pó (extintores "secos"). Esta substância é também fornecida em cristais verde esmeralda ou água-marinha em conjuntos de crescimentos de cristais ("aquários químicos") com fins educativos ou recreacionais.
PRODUÇÃO [3] editar
“O mono amónio fosfato … é produzido por reação de amónia anidra e ácido fosfórico em reatores descontínuos ou contínuos e cristalizado em cristalizadores convencionais porque a pressão parcial de amónia sobre esta solução ácida é relativamente baixa. Os cristais são centrifugados e secos abaixo de 100 ° C num secador rotativo e a água-mãe é devolvida ao reator.”
“Os mono amónio fosfato são produzidos pela neutralização do ácido fosfórico com amónia. O ácido fosfórico húmido bruto ou parcialmente purificado é usado principalmente para aplicações em fertilizantes. No entanto, o ácido fosfórico térmico puro é usado preferencialmente para a produção de fosfatos de amónio comerciais com um ensaio > 99%.”
“Bombeando gás de amónia seco numa solução a 80% de ácido fosfórico. A composição do produto é controlada mantendo o pH entre 3,8 e 4,5. Quando a mistura é arrefecida, cristais de fosfato mono amónio precipitam.”
USOS editar
FERTILIZANTE - GRANULADO MONO AMÓNIO FOSFATO [4][5][6] editar
Este granulado é para uso directo, que contém fósforo e nitrogénio. O fósforo é totalmente solúvel em água, e todo o nitrogénio está na forma amoniacal. É um fertilizante universal que pode ser usado em todos os tipos de culturas e de solo. Ele é especialmente adequado como fertilizante em culturas com uma alta exigência de fósforo (por exemplo, milho). Além disso, a absorção de fósforo pelas raízes é também potenciada pelo alto teor de nitrogénio amoniacal.
FERTILIZANTE - SAL MONO AMÓNIO FOSFATO [4][5][6] editar
Este sal é um cristal branco, onde se diluí em água. Tal como o fertilizante granulado contém nitrogénio e fósforo. Sendo utilizado também para todos os tipos de solo e culturas.
EXTINTOR - PÓ MONO AMÓNIO FOSFATO [7][8][9][10] editar
Este pó é utilizado em extintores contra incêndios de classe A, B e C. Eles contêm mono amónio fosfato, que sai como um pó amarelo, e ao aplicar-se, as partículas fundem-se e dilatam-se, forma uma barreira que evita a entrada de oxigénio completando todo o processo de extinção.
É utilizado nos incêndios em madeira, papel, tecido, plásticos, líquidos inflamáveis e gases combustíveis.
OUTROS USOS [3] editar
Aditivos alimentares.
Fermento em pó.
Retardam as chamas em vários materiais de madeira e papel.
Aplicações em cerâmica e sondas subaquáticas.
Usos em química analítica.
CUIDADOS NO MANUSEAMENTO [3][7][11][8][10] editar
Independentemente do seu uso verificar sempre a identificação e armazenagem
- USO DE EPIS - Equipamento de protecção individuais.
- NO CASO DE USO AGRÍCOLA - Aconselha-se a máscara, roupa que cubra todo o corpo, luvas e viseira.
- NO CASO DE USO DE EXTINTOR - Utilizar protecção de bombeiro, se não for possível, tapar a boca com tecido ou suster a respiração. Manter uma distância de segurança de 2 metros.
- NO CASO DE USO ALIMENTAR - Ter o cuidado de usar as doses corretas e nunca ultrapassar esses valores.
Referências
- ↑ Lide, David R. (1998). Handbook of Chemistry and Physics 87 ed. Boca Raton, FL: CRC Press. pp. 4–40. ISBN 0-8493-0594-2
- ↑ a b c d Registo de CAS RN 7722-76-1 na Base de Dados de Substâncias GESTIS do IFA
- ↑ a b c National Center for Biotechnology Information. PubChem Database. AMMONIUM DIHYDROGEN PHOSPHATE, Source=HSDB, https://pubchem.ncbi.nlm.nih.gov/source/hsdb/1229#section=Methods-of-Manufacturing (accessed on Apr. 16, 2020)
- ↑ a b "Monoammonium Phosphate (MAP)", The Mosaic Company, Acedido em https://www.cropnutrition.com/resource-library/monoammonium-phosphate-map - Consultado a 27/03/2020
- ↑ a b Agropolychim (2016). "Monoammonium Phosphate (MAP)" https://agropolychim.bg/wp-content/uploads/2016/06/map_esds_en-june-2016.pdf
- ↑ a b Haifa "Monoammonium Phosphate" https://www.kirbyagri.com/downloads/fertilizer-sheets/map%20sds.pdf
- ↑ a b Dry Chemical Powder Type (Stored Pressure), Bharati Fire Engineers, Acedido em https://www.bharatifire.com/Firefite_Extinguisher_Dry-chemical-powder.php - Consultado a 27/03/2020
- ↑ a b Fire Extinguisher Safety, Poison Control NCPC, Acedido em https://www.poison.org/articles/fire-extinguisher-safety-184 Consultado a 27/03/2020
- ↑ Santa Cruz Biotechnology "Ammonium Phosphate Monobasic" http://datasheets.scbt.com/sc-202948.pdf
- ↑ a b National Research Council (US) Subcommittee on Flame-Retardant Chemicals. Toxicological Risks of Selected Flame-Retardant Chemicals. Washington (DC): National Academies Press (US); 2000. 12, Ammonium Polyphosphates. Available from: https://www.ncbi.nlm.nih.gov/books/NBK225644/
- ↑ "Monoammonium Phosphate (MAP)", The Mosaic Company, Acedido em https://www.cropnutrition.com/resource-library/monoammonium-phosphate-map - Consultado a 27/03/2020