Fosfatidiletanolamina
| Fosfatidiletanolamina Alerta sobre risco à saúde | |
|---|---|
| |
| Identificadores | |
| Número CAS | |
| MeSH | |
| Página de dados suplementares | |
| Estrutura e propriedades | n, εr, etc. |
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas |
| Dados espectrais | UV, IV, RMN, EM |
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |
A fostatidiletanolamina é um glicofosfolipídeo, que é um derivado do composto precursor ácido fosfatídico, de acordo com o álcool polar no seu grupo-cabeça.
Por exemplo, a fosfatidilcolina e fosfatidiletanolamina tem colina e etanolamina nos seus grupos-cabeça polares. Em todos esses compostos, o grupo-cabeça esta ligado ao glicerol por um fosfodiéster, no qual o grupo fosfato tem uma carga negativa em pH neutro. O álcool polar pode estar negativamente carregado (como no fosfatidillinositol 4,5 bifosfato), neutro (fosfatidilserina) ou positivamente carregado (fosfaticilcolina, fostatidiletanolamina). Essas cargas tem uma contribuição significante nas propriedades de superfície das membranas.
A S-Adenosil metionina pode subsequentemente metilar a amina de fosfatidiletanolaminas para produzir fosfatidilcolinas. Pode encontrar-se principalmente na região interna (citoplasmática) da bicamada lipídica.[1]
Funções
editarEm células
editarAs fosfatidiletanolaminas são encontradas em todas as células vivas, compondo 25% de todos os fosfolípidos. Na fisiologia humana, eles são encontrados particularmente em tecidos nervosos, como a substância branca do cérebro, nervos, tecido neural e na medula espinhal, onde compõem 45% de todos os fosfolípidos.[2]
As fosfatidiletanolaminas desempenham um papel na fusão da membrana e na desmontagem do anel contrátil durante a citocinese na divisão celular.[3] Além disso, pensa-se que a fosfatidiletanolamina regula a curvatura da membrana. A fosfatidiletanolamina é um importante precursor, substrato ou doador em várias vias biológicas.[2]
Como um grupo de cabeça polar, a fosfatidiletanolamina cria uma membrana lipídica mais viscosa em comparação com a fosfatidilcolina. Por exemplo, a temperatura de fusão da di-oleoil-fosfatidiletanolamina é de -16 °C enquanto a temperatura de fusão da di-oleoil-fosfatidilcolina é de -20 °C. Se os lípidos tivessem duas cadeias de palmitoil, a fosfatidiletanolamina fundiria a 63 °C, enquanto a fosfatidilcolina derreteria já a 41 °C.[4] As temperaturas de fusão inferior correspondem, em uma visão simplista, a membranas mais fluidas.
Em humanos
editarEm seres humanos, o metabolismo da fosfatidiletanolamina é considerado importante no coração, pois quando o fluxo de sangue para o coração é restrito, a distribuição assimétrica da fosfatidiletanolamina entre os folhetos da membrana é interrompida e, como resultado, a membrana é interrompida. Além disso, a fosfatidiletanolamina desempenha um papel na secreção de lipoproteínas no fígado. Isso ocorre porque as vesículas para a secreção de lipoproteínas de baixa densidade que surgem do Golgi possuem uma concentração de fosfatidiletanolamina significativamente maior quando comparada a outras vesículas contendo lipoproteínas de baixa densidade.[5]
A fosfatidiletanolamina também mostrou poder propagar priões infecciosos sem a ajuda de proteínas ou ácidos nucleicos, o que é uma característica única dela[6]. É também pensado que a fosfatidiletanolamina desempenha um papel na coagulação do sangue, pois funciona com fosfatidilserina no aumento da taxa de formação de trombina promovendo a ligação ao fator V e ao fator X, duas proteínas que catalisam a formação da trombina a partir da protrombina.[7]
Em bactérias
editarOnde a fosfatidilcolina é o principal fosfolípido em animais, a fosfatidiletanolamina é a principal em bactérias. Um dos principais papéis da fosfatidiletanolamina nas membranas bacterianas é espalhar a carga negativa causada por fosfolípidos de membrana aniônica. Na bactéria Escherichia coli, a fosfatidiletanolamina desempenha um papel no apoio à permeases da lactose, ao transporte ativo de lactose na célula e também pode desempenhar um papel em outros sistemas de transporte. A fosfatidiletanolamina desempenha um papel na montagem da permease da lactose e outras proteínas de membrana. Ele atua como um "acompanhante" para ajudar as proteínas da membrana a dobrar corretamente suas estruturas terciárias para que possam funcionar corretamente. Quando a fosfatidiletanolamina não está presente, as proteínas de transporte têm estruturas terciárias incorretas e não funcionam corretamente.[8]
A fosfatidiletanolamina também permite que os transportadores multidrogas bacterianos funcionem adequadamente, e permite a formação de intermediários que são necessários para que os transportadores abram e fechem corretamente.[9]
Estrutura
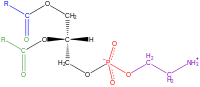
editarPor ser uma lecitina, (uma mistura de glicolípidios, triglicerídios e fosfolipídios), a fostatidiletanolamina consiste em uma combinação de glicerol esterificado com dois ácidos graxos e ácido fosfórico.
Considerando que o grupo fosfato é combinado com colina em fosfatidilcolina, e combinado com a etanolamina em fosfatidiletanolamina. Os dois ácidos gordurosos podem ser iguais ou diferentes, e geralmente estão nas 1,2 posições (embora possam estar nas 1,3 posições).
Sínteses
editarA via de descarboxilação de fosfatidilserina e as vias de difenossulfato-etanolamina de citidina são utilizadas para sintetizar a fosfatidiletanolamina.
A fosfatidilserina descarboxilase é a enzima que é usada para descarboxilação de fosfatidilserina no primeiro caminho.
A via de descarboxilação de fosfatidilserina é a principal fonte de síntese para fosfatidiletanolamina nas membranas das mitocôndrias. A fosfatidiletanolamina produzida na membrana mitocondrial também é transportada por toda a célula para outras membranas para uso.
Em um processo que reflete a síntese de fosfatidilcolina, a fosfatidiletanolamina também é feita através da via de difenossulfato-etanolamina citidina, utilizando-se a etanolamina como substrato. Através de várias etapas que ocorrem tanto no citosol quanto no retículo endoplasmático, o caminho de síntese produz o produto final da fosfatidiletanolamina.[10] A fosfatidiletanolamina também é encontrada abundantemente em lecitina de soja ou ovo e é produzida comercialmente usando separação cromatográfica.
Regulação
editarA síntese de fosfatidiletanolamina através da via de descarboxilação de fosfatidilserina ocorre rapidamente na membrana mitocondrial interna. No entanto, a fosfatidilserina é feita no retículo endoplasmático. Por isso, ocorre o transporte de fosfatidilserina do retículo endoplasmático para a membrana mitocondrial e, em seguida, para a membrana mitocondrial interna, que limita a taxa de síntese através desta via. O mecanismo para este transporte é atualmente desconhecido, mas pode desempenhar um papel na regulação da taxa de síntese nesta via.
Presença em alimentos, problemas de saúde
editarAs fosfatidiletanolaminas em alimentos se fragmentam para formar ‘produtos Amadori’ ligados à fosfatidiletanolamina como parte da reação de Maillard.[11]
Esses produtos aceleram a peroxidação lipídica das membranas, causando estresse oxidativo para as células que entram em contato com elas.[12] O estresse oxidativo é conhecido por causar deterioração de alimentos e várias doenças. Foram encontrados níveis significativos de produtos de Amadori-fosfatidiletanolamina em uma grande variedade de alimentos, como chocolate, leite de soja, fórmula infantil e outros alimentos processados. Os níveis de produtos Amadori-fosfatidiletanolamina são maiores em alimentos com altas concentrações de lipídios e açúcares que apresentam altas temperaturas no processamento.[11] Estudos adicionais descobriram que Amadori-fosfatidiletanolamina pode desempenhar um papel na doença vascular,[13] atuam como o mecanismo pelo qual o diabetes pode aumentar a incidência de câncer [14] e também pode desempenhar um papel importante em outras doenças. A amadori-fosfatidiletanolamina tem uma maior concentração plasmática em pacientes com diabetes do que pessoas saudáveis, indicando que pode desempenhar um papel no desenvolvimento da doença ou ser um produto da doença.[15]
- ↑ Wellner, Niels; Diep, Thi Ai; Janfelt, Christian; Hansen, Harald Severin (março 2013). «N-acylation of phosphatidylethanolamine and its biological functions in mammals». Biochimica Et Biophysica Acta. 1831 (3): 652–662. ISSN 0006-3002. PMID 23000428. doi:10.1016/j.bbalip.2012.08.019
- ↑ a b Vance, Jean E.; Tasseva, Guergana (março 2013). «Formation and function of phosphatidylserine and phosphatidylethanolamine in mammalian cells». Biochimica Et Biophysica Acta. 1831 (3): 543–554. ISSN 0006-3002. PMID 22960354. doi:10.1016/j.bbalip.2012.08.016
- ↑ Emoto, K.; Kobayashi, T.; Yamaji, A.; Aizawa, H.; Yahara, I.; Inoue, K.; Umeda, M. (12 de novembro de 1996). «Redistribution of phosphatidylethanolamine at the cleavage furrow of dividing cells during cytokinesis». Proceedings of the National Academy of Sciences of the United States of America. 93 (23): 12867–12872. ISSN 0027-8424. PMID 8917511
- ↑ Veja referências em Wan et al. Biochemistry 47 2008
- ↑ Vance, Jean E. (julho 2008). «Phosphatidylserine and phosphatidylethanolamine in mammalian cells: two metabolically related aminophospholipids». Journal of Lipid Research. 49 (7): 1377–1387. ISSN 0022-2275. PMID 18204094. doi:10.1194/jlr.R700020-JLR200
- ↑ Deleault, Nathan R.; Piro, Justin R.; Walsh, Daniel J.; Wang, Fei; Ma, Jiyan; Geoghegan, James C.; Supattapone, Surachai (29 de maio de 2012). «Isolation of phosphatidylethanolamine as a solitary cofactor for prion formation in the absence of nucleic acids». Proceedings of the National Academy of Sciences of the United States of America. 109 (22): 8546–8551. ISSN 1091-6490. PMID 22586108. doi:10.1073/pnas.1204498109
- ↑ Majumder, Rinku; Liang, Xiaoe; Quinn-Allen, Mary Ann; Kane, William H.; Lentz, Barry R. (14 de outubro de 2011). «Modulation of prothrombinase assembly and activity by phosphatidylethanolamine». The Journal of Biological Chemistry. 286 (41): 35535–35542. ISSN 1083-351X. PMID 21859710. doi:10.1074/jbc.M111.260141
- ↑ Christie, W.W. (April 16, 2012). "Phosphatidylethanolamine and Related Lipids". The AOCS Lipid Library. Retrieved September 3, 2012. «Título ainda não informado (favor adicionar)»
- ↑ Gbaguidi, B.; Hakizimana, P.; Vandenbussche, G.; Ruysschaert, J.-M. (junho 2007). «Conformational changes in a bacterial multidrug transporter are phosphatidylethanolamine-dependent». Cellular and molecular life sciences: CMLS. 64 (12): 1571–1582. ISSN 1420-682X. PMID 17530171. doi:10.1007/s00018-007-7031-0
- ↑ Kelly, Karen (July 28, 2011). "Phospholipid Biosynthesis". The AOCS Lipid Library. Retrieved September 3, 2012. «Título ainda não informado (favor adicionar)»
- ↑ a b Oak, Jeong-Ho; Nakagawa, Kiyotaka; Miyazawa, Teruo (março 2002). «UV analysis of Amadori-glycated phosphatidylethanolamine in foods and biological samples». Journal of Lipid Research. 43 (3): 523–529. ISSN 0022-2275. PMID 11893788
- ↑ Oak, J.; Nakagawa, K.; Miyazawa, T. (8 de setembro de 2000). «Synthetically prepared Aamadori-glycated phosphatidylethanolaminecan trigger lipid peroxidation via free radical reactions». FEBS letters. 481 (1): 26–30. ISSN 0014-5793. PMID 10984609
- ↑ Oak, Jeong-Ho; Nakagawa, Kiyotaka; Oikawa, Shinichi; Miyazawa, Teruo (4 de dezembro de 2003). «Amadori-glycated phosphatidylethanolamine induces angiogenic differentiations in cultured human umbilical vein endothelial cells». FEBS letters. 555 (2): 419–423. ISSN 0014-5793. PMID 14644453
- ↑ Eitsuka, Takahiro; Nakagawa, Kiyotaka; Ono, Yuichi; Tatewaki, Naoto; Nishida, Hiroshi; Kurata, Tadao; Shoji, Naoki; Miyazawa, Teruo (30 de julho de 2012). «Amadori-glycated phosphatidylethanolamine up-regulates telomerase activity in PANC-1 human pancreatic carcinoma cells». FEBS letters. 586 (16): 2542–2547. ISSN 1873-3468. PMID 22750441. doi:10.1016/j.febslet.2012.06.027
- ↑ Ariizumi, Ken; Koike, Tomoyuki; Ohara, Shuichi; Inomata, Yoshifumi; Abe, Yasuhiko; Iijima, Katsunori; Imatani, Akira; Oka, Yoshitomo; Shimosegawa, Tooru (28 de maio de 2008). «Incidence of reflux esophagitis and Helicobacter pylori infection in diabetic patients». World Journal of Gastroenterology : WJG. 14 (20): 3212–3217. ISSN 1007-9327. PMID 18506928. doi:10.3748/wjg.14.3212