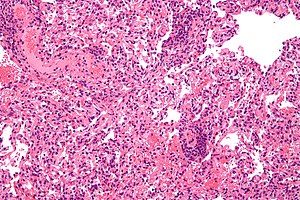
Rejeição de transplante
A rejeição do transplante ocorre quando o tecido transplantado é rejeitado pelo sistema imunológico do receptor, que destrói o tecido transplantado. A rejeição do transplante pode ser diminuída pela determinação da semelhança molecular entre doador e receptor e pelo uso de medicamentos imunossupressores após o transplante.[1][2]
| Rejeição de transplante | |
|---|---|
| Micrografia onde se observa a rejeição de um transplante de pulmão | |
| Classificação e recursos externos | |
| CID-10 | T86 |
| CID-11 | 129221830 |
| MedlinePlus | 000815 |
| MeSH | D006084 |
Tipos de rejeição de transplante
editarA rejeição do transplante pode ser classificada em três tipos: hiperaguda, aguda e crônica. Esses tipos são diferenciados pela rapidez com que o sistema imunológico do receptor é ativado e pelo aspecto ou aspectos específicos da imunidade envolvidos.[3]
Rejeição hiperaguda
editarA Rejeição hiperaguda é uma forma de rejeição que se manifesta minutos a horas após o transplante.[4] É causada pela presença de anticorpos preexistentes no receptor que reconhecem antígenos no órgão doador.[5] Esses antígenos estão localizados no revestimento endotelial dos vasos sanguíneos do órgão transplantado e, uma vez que os anticorpos se liguem, levarão à rápida ativação do sistema do complemento.[6] São esperados danos irreversíveis através de trombose e subsequente necrose do enxerto. O tecido deixado implantado não funcionará e poderá causar febre alta e mal-estar, pois o sistema imunológico atua contra o tecido estranho.[7][8]
Rejeição Aguda
editarA Rejeição aguda é uma categoria de rejeição que ocorre na escala de semanas a meses, com a maioria dos episódios ocorrendo nos primeiros 3 meses a 1 ano após o transplante.[6] Ao contrário da rejeição hiperaguda, pensa-se que a rejeição aguda surge de dois mecanismos imunológicos distintos, à medida que os linfócitos, um subconjunto de glóbulos Brancos, começam a reconhecer antígenos no órgão/enxerto transplantado.[9] Esse reconhecimento ocorre devido ao complexo principal de histocompatibilidade (MHC), que são proteínas na superfície celular que são apresentadas ao receptor de células T encontrado nas células T.[10] Em humanos, isso é conhecido como sistema de antígeno leucocitário humano (HLA) e mais de 17.000 alelos HLA ou variantes genéticas foram descritos, de modo que é extremamente incomum que duas pessoas tenham alelos idênticos.[11] Outras proteínas não-HLA, conhecidas como antígenos de histocompatibilidade menores, existem, mas geralmente são incapazes de causar rejeição aguda por si mesmas, a menos que uma infinidade de proteínas não-HLA sejam incompatíveis. Como tal, a correspondência HLA (além da correspondência dos grupos ABO) é crítica na prevenção da rejeição aguda.[12][13]
Este processo de reconhecimento pelas células T pode acontecer direta ou indiretamente e levar à rejeição celular aguda e à rejeição humoral aguda, respectivamente.[6] O aloreconhecimento direto é um fenômeno dentro da imunologia do transplante, onde as células dendríticas, que são as células apresentadoras de antígenos do corpo, migram do tecido doador para o tecido linfóide (folículos linfóides e nódulos linfáticos) no receptor e apresentam seus peptídeos MHC aos linfócitos receptores.[14] Em comparação, o aloreconhecimento indireto é mais análogo ao modo como os antígenos estranhos são reconhecidos pelo sistema imunológico. As células dendríticas do receptor encontram peptídeos do tecido do doador, seja na circulação, no tecido linfóide ou no próprio tecido do doador. Dado que não são o resultado da apresentação direta do antígeno, estas podem não ser necessariamente moléculas intactas do MHC, mas em vez disso, outras proteínas que são consideradas suficientemente diferentes do receptor podem gerar uma resposta. Este processo leva à preparação das células T para responder secundariamente aos peptídeos daqui para frente. Uma terceira via semidireta foi descrita na qual as APCs receptoras apresentam MHCs de doadores totalmente intactos, mas sua contribuição relativa para a rejeição aguda não é tão bem compreendida.[14][15]
Rejeição Crônica
editarA Rejeição crônica é uma forma insidiosa de rejeição que leva à destruição do enxerto ao longo de meses, mas na maioria das vezes anos após o transplante de tecido.[9] O mecanismo de rejeição crónica ainda não está totalmente compreendido, mas sabe-se que episódios prévios de rejeição aguda são o principal preditor clínico para o desenvolvimento de rejeição crónica.[6] Em particular, a incidência aumenta após rejeição aguda grave ou persistente, enquanto episódios de rejeição aguda com retorno à função inicial não têm efeitos importantes na sobrevivência do enxerto.[16][17] A rejeição crónica é geralmente considerada como estando relacionada com danos vasculares ou danos parenquimatosos com subsequente fibrose.[18] Embora seja desconhecida a contribuição exata do sistema imunitário nestes processos, a via indireta do aloreconhecimento e a formação de anticorpos associada parecem estar especialmente envolvidas.[6]
A rejeição crônica tem efeitos amplamente variados em diferentes órgãos. Cinco anos após o transplante, 80% dos transplantes de pulmão, 60% dos transplantes de coração e 50% dos transplantes de rim são afetados, enquanto os transplantes de fígado são afetados apenas 10% das vezes.[16] Portanto, a rejeição crônica explica a morbidade a longo prazo na maioria dos receptores de transplante de pulmão, a sobrevida média de aproximadamente 4,7 anos, cerca de metade do período em comparação com outros transplantes de órgãos importantes.[19][20] A obstrução do fluxo aéreo não atribuível a outra causa é denominada síndrome de bronquiolite obliterante (BOS), confirmada por uma queda persistente – três ou mais semanas – no volume expiratório forçado (VEF1) em pelo menos 20%. Primeiramente notada é a infiltração de linfócitos, seguida por lesão de células epiteliais, depois lesões inflamatórias e recrutamento de fibroblastos e miofibroblastos, que proliferam e secretam proteínas formando tecido cicatricial. Um fenômeno semelhante pode ser observado no transplante de fígado, em que a fibrose leva à icterícia secundária à destruição dos ductos biliares no fígado, também conhecida como síndrome do desaparecimento dos ductos biliares.[21]
Rejeição por não adesão
editarUma das principais razões para a rejeição do transplante é a não adesão aos regimes imunossupressores prescritos. Este é particularmente o caso dos receptores adolescentes, com taxas de não adesão próximas dos 50% em alguns casos.[22]
Referências
editar- ↑ Frohn C, Fricke L, Puchta JC, Kirchner H (Fevereiro de 2001). «The effect of HLA-C matching on acute renal transplant rejection». Nephrology, Dialysis, Transplantation. 16 (2): 355–360. PMID 11158412. doi:10.1093/ndt/16.2.355
- ↑ «Considerações gerais sobre transplantes - Doenças imunológicas». Manual MSD Versão Saúde para a Família. Consultado em 5 de outubro de 2023
- ↑ Moreau A, Varey E, Anegon I, Cuturi MC (Novembro de 2013). «Effector mechanisms of rejection». Cold Spring Harbor Perspectives in Medicine. 3 (11): a015461. PMC 3808773 . PMID 24186491. doi:10.1101/cshperspect.a015461
- ↑ Chang YC (1 de janeiro de 2021). «The surgical and immunosuppressive basis for infections in the pediatric solid organ transplant recipient». In: Steinbach WJ, Green MD, Michaels MG, Danziger-Isakov LA. Pediatric Transplant and Oncology Infectious Diseases (em inglês). Philadelphia: Elsevier. pp. 1–9.e3. ISBN 978-0-323-64198-2. doi:10.1016/B978-0-323-64198-2.00010-5
- ↑ Harmon WE (1 de janeiro de 2010). «Chapter 41 - Pediatric Renal Transplantation». In: Himmelfarb J, Sayegh MH. Chronic Kidney Disease, Dialysis, and Transplantation (em inglês) Third ed. Philadelphia: W.B. Saunders. pp. 591–608. ISBN 978-1-4377-0987-2. doi:10.1016/B978-1-4377-0987-2.00041-8
- ↑ a b c d e Mak TW, Saunders ME, Jett BD, eds. (1 de janeiro de 2014). «Chapter 17 - Transplantation». Primer to the Immune Response (em inglês) Second ed. Boston: Academic Cell. pp. 457–486. ISBN 978-0-12-385245-8. doi:10.1016/B978-0-12-385245-8.00017-0
- ↑ Dharnidharka VR (1 de janeiro de 2019). «43 - Pediatric Renal Transplantation». In: Himmelfarb J, Ikizler TA. Chronic Kidney Disease, Dialysis, and Transplantation (em inglês) Fourth ed. Philadelphia: Elsevier. pp. 661–675.e7. ISBN 978-0-323-52978-5. doi:10.1016/B978-0-323-52978-5.00043-4
- ↑ Vitak K (1 de janeiro de 2014). «Chapter 14 - Organ Transplantation». In: Paz JC, West MP. Acute Care Handbook for Physical Therapists (em inglês) Fourth ed. St. Louis: W.B. Saunders. pp. 335–356. ISBN 978-1-4557-2896-1. doi:10.1016/B978-1-4557-2896-1.00014-7
- ↑ a b Justiz Vaillant AA, Mohseni M (2022). «Chronic Transplantation Rejection». StatPearls. Treasure Island (FL): StatPearls Publishing. PMID 30571056. Consultado em 16 de março de 2022
- ↑ Delves PJ. «Human Leukocyte Antigen (HLA) System - Immunology; Allergic Disorders». Merck Manuals Professional Edition (em inglês). Merck & Co. Consultado em 30 de Setembro de 2020
- ↑ Frenet EM, Scaradavou A (1 de janeiro de 2019). «Chapter 32 - Human Leukocyte Antigens». In: Shaz BH, Hillyer CD, Gil MR. Transfusion Medicine and Hemostasis (em inglês) Third ed. [S.l.]: Elsevier. pp. 191–197. ISBN 978-0-12-813726-0. doi:10.1016/B978-0-12-813726-0.00032-5
- ↑ Menon MC, Cravedi P, El Salem F (1 de janeiro de 2017). «Chapter 32 - Acute Cellular Rejection». In: Orlando G, Remuzzi G, Williams DF. Kidney Transplantation, Bioengineering and Regeneration (em inglês). [S.l.]: Academic Press. pp. 461–474. ISBN 978-0-12-801734-0. doi:10.1016/B978-0-12-801734-0.00032-1
- ↑ Justiz Vaillant AA, Misra S, Fitzgerald BM (2022). «Acute Transplantation Rejection». StatPearls. Treasure Island (FL): StatPearls Publishing. PMID 30571031. Consultado em 16 de março de 2022
- ↑ a b Boardman DA, Jacob J, Smyth LA, Lombardi G, Lechler RI (2016). «What Is Direct Allorecognition?». Current Transplantation Reports. 3 (4): 275–283. PMC 5107184 . PMID 27909647. doi:10.1007/s40472-016-0115-8
- ↑ Ingulli E (Janeiro de 2010). «Mechanism of cellular rejection in transplantation». Pediatric Nephrology. 25 (1): 61–74. PMC 2778785 . PMID 21476231. doi:10.1007/s00467-008-1020-x
- ↑ a b Gautreaux MD (1 de janeiro de 2017). «Chapter 17 - Histocompatibility Testing in the Transplant Setting». In: Orlando G, Remuzzi G, Williams DF. Kidney Transplantation, Bioengineering and Regeneration (em inglês). [S.l.]: Academic Press. pp. 223–234. ISBN 978-0-12-801734-0. doi:10.1016/b978-0-12-801734-0.00017-5
- ↑ Srinivas TR, Schold JD, Meier-Kriesche HU (1 de janeiro de 2010). «Chapter 105 - Outcomes of Renal Transplantation». In: Floege J, Johnson RJ, Feehally J. Comprehensive Clinical Nephrology (em inglês) Fourth ed. Philadelphia: Mosby. pp. 1222–1231. ISBN 978-0-323-05876-6. doi:10.1016/b978-0-323-05876-6.00105-2
- ↑ Dharnidharka VR (1 de janeiro de 2019). «Chapter 43 - Pediatric Renal Transplantation». In: Himmelfarb J, Ikizler TA. Chronic Kidney Disease, Dialysis, and Transplantation (em inglês) Fourth ed. Philadelphia: Elsevier. pp. 661–675.e7. ISBN 978-0-323-52978-5. doi:10.1016/B978-0-323-52978-5.00043-4
- ↑ Jaramillo A, Fernández FG, Kuo EY, Trulock EP, Patterson GA, Mohanakumar T (Fevereiro de 2005). «Immune mechanisms in the pathogenesis of bronchiolitis obliterans syndrome after lung transplantation». Pediatric Transplantation. 9 (1): 84–93. PMID 15667618. doi:10.1111/j.1399-3046.2004.00270.x
- ↑ Lau CL, Patterson GA (Novembro de 2003). «Current status of lung transplantation». The European Respiratory Journal. Supplement. 47: 57s–64s. PMID 14621118. doi:10.1183/09031936.03.00022103
- ↑ Hübscher SG, Clouston AD (Janeiro de 2012). «Chapter 15 - Transplantation pathology». In: Burt AD, Portmann BC, Ferrell LD. MacSween's Pathology of the Liver (em inglês) Sixth ed. Edinburgh: Churchill Livingstone. pp. 853–933. ISBN 978-0-7020-3398-8. doi:10.1016/B978-0-7020-3398-8.00015-5
- ↑ Dobbels F, Hames A, Aujoulat I, Heaton N, Samyn M (Fevereiro de 2012). «Should we retransplant a patient who is non-adherent? A literature review and critical reflection». Pediatric Transplantation. 16 (1): 4–11. PMID 22248250. doi:10.1111/j.1399-3046.2011.01633.x