Bombicol
O bombicol é um feromônio liberado pela mariposa do bicho-da-seda para atrair parceiros. É também o feromônio sexual da mariposa da seda selvagem (Bombyx mandarina).[1][2] Descoberto por Adolf Butenandt em 1959, foi o primeiro feromônio a ser caracterizado quimicamente.[3]
Quantidades minúsculas deste feromônio podem ser usadas por acre de terra para confundir os insetos machos sobre a localização de suas parceiras. Assim, pode servir como isca em armadilhas para remover os insetos de forma eficaz sem pulverizar as culturas com grandes quantidades de pesticidas. Butenandt nomeou a substância após o nome latino da mariposa Bombyx mori.[4]
In vivo, parece que o bombicol é o ligante natural para uma proteína de ligação de feromônio, BmorPBP, que acompanha o feromônio ao receptor de feromônio.[5]
Biossíntese
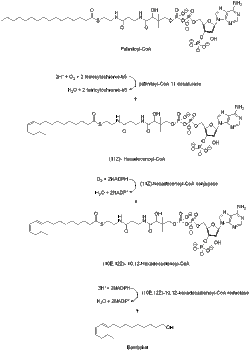
editarO bombicol é conhecido por ser derivado de acetil-CoA através do acil graxo C-16 palmitoil-CoA.[6] O palmitoil-CoA é convertido em bombicol em etapas que envolvem dessaturação e modificação redutiva do carbono carbonílico.[7] Em comparação com outros feromônios do Tipo I, a biossíntese de bombicol não precisa de encurtamento de cadeia ou qualquer outro tipo de modificação do grupo hidroxila terminal.
Uma enzima dessaturase, codificada pelo gene Bmpgdesat1 (Desat1), produz o monoeno (11Z)-hexadecenoil-CoA bem como o dieno (10E,12Z)-10,12-hexadecadienoil-CoA. Essa dessaturase é a única enzima necessária para catalisar essas duas etapas consecutivas de dessaturação.[8]
O precursor de bombicol acil (10E,12Z)-10,12-hexadecadienoato é encontrado principalmente como um éster de triacilglicerol nas gotículas lipídicas citoplasmáticas das células da glândula de feromônio da mariposa. E quando as fêmeas adultas emergem de suas pupas, o neurohormônio PBAN (neuropeptídeo ativador da biossíntese de feromônios) começa a sinalizar eventos que ajudam a controlar a lipólise dos triacilgliceróis armazenados, liberando (10E,12Z)-10,12-hexadecadienoato para sua final modificação redutiva.[9][10][11] O mecanismo de liberação lipolítica de (10E,12Z)-10,12-hexadecadienoato de triacilgliceróis não é completamente conhecido, mas os genes codificadores de lipase candidatos foram identificados.[9][10]
Referências
- ↑ Kuwahara, Yasumasa (1984). «Flight Time of Bombyx mandarina Males to a Pheromone Trap Baited with Bombykol». Applied Entomology and Zoology. 19 (3): 400–401. doi:10.1303/aez.19.400
- ↑ Kuwahara, Yasumasa; Mori, Naoki; Yamada, Shigeki; Nemoto, Tadashi (1984). «Evaluation of Bombykol as the Sex Pheromone of Bombyx mandarina(Lepidoptera : Bombycidae)». Applied Entomology and Zoology. 19 (2): 265–267. doi:10.1303/aez.19.265
- ↑ Butenandt, A.; Beckamnn, R.; Hecker, E. (1961). «Über den Sexuallockstoff des Seidenspinners .1. Der biologische Test und die Isolierung des reinen Sexuallockstoffes Bombykol». Hoppe-Seyler's Zeitschrift für Physiologische Chemie. 324: 71–83. PMID 13689417. doi:10.1515/bchm2.1961.324.1.71
- ↑ «Molecule of the Week». American Chemical Society. 2004. Consultado em 2 de março de 2013. Arquivado do original em 7 de agosto de 2004
- ↑ Leal, Walter S. (2005). «Pheromone Reception». In: Schulz, Stefan. The Chemistry of Pheromones and Other Semiochemicals II. Col: Topics in Current Chemistry. 240. [S.l.]: Springer. pp. 1–36. ISBN 9783540213086. doi:10.1007/b98314. Consultado em 2 de março de 2013
- ↑ Caspi et al, Nucleic Acids Research 42:D459-D471 2014.
- ↑ Ando, T; Hase, T; Arima, R; Uchiyama, M (1988). «Biosynthetic pathway of bombykol, the sex pheromone of the female silkworm moth». Agricultural and Biological Chemistry. 52 (2): 473–478. doi:10.1271/bbb1961.52.473
- ↑ Moto, K; Suzuki, MG; Hull, JJ; Kurata, R; Takahashi, S; Yamamoto, M; Okano, K; Imai, K; Ando, T; Matsumoto, S (2004). «Involvement of a bifunctional fatty-acyl desaturase in the biosynthesis of the silkmoth, Bombyx mori, sex pheromone». Proceedings of the National Academy of Sciences. 101 (23): 8631–6. Bibcode:2004PNAS..101.8631M. PMC 423246 . PMID 15173596. doi:10.1073/pnas.0402056101
- ↑ a b Zhang, SD; Li, X; Bin, Z; Du, MF; Yin, XM; An, SH (2014). «Molecular identification of a pancreatic lipase-like gene involved in sex pheromone biosynthesis of Bombyx mori». Insect Science. 21 (4): 459–68. PMID 23955937. doi:10.1111/1744-7917.12053
- ↑ a b Ohnishi, A; Kaji, M; Hashimoto, K; Matsumoto, S (2011). «Screening for the Genes Involved in Bombykol Biosynthesis: Identification and Functional Characterization of Bombyx mori Acyl Carrier Protein». Frontiers in Endocrinology. 2: 92. PMC 3355880 . PMID 22649392. doi:10.3389/fendo.2011.00092
- ↑ Matsumoto, S; Ozawa, R; Uchiumi, K; Kurihara, M (1996). «Cell-free production of the silkworm sex pheromone bombykol». Bioscience, Biotechnology, and Biochemistry. 60 (2): 369–73. PMID 9063992. doi:10.1271/bbb.60.369