Tiocianato de potássio
| Tiocianato de potássio Alerta sobre risco à saúde | |
|---|---|
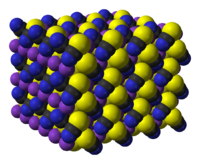
| |
| Outros nomes | Potassium sulfocyanate Potassium isothiocyanate Potassium thiocyanide Potassium rhodanide |
| Identificadores | |
| Número CAS | |
| PubChem | |
| ChemSpider | |
| ChEBI | |
| Número RTECS | XL1925000 |
| SMILES |
|
| InChI | 1/CHNS.K/c2-1-3;/h3H;/q;+1/p-1
|
| Propriedades | |
| Fórmula molecular | KSCN |
| Massa molar | 97.181 g mol−1 |
| Aparência | Cristais incolores deliquescentes |
| Odor | Odorless |
| Densidade | 1.886 g/cm3 |
| Ponto de fusão |
173.2 °C, 446 K, 344 °F |
| Ponto de ebulição |
500 °C, 773 K, 932 °F |
| Solubilidade em água | 177 g/100 mL (0 °C) 217 g/100 mL (20 °C) |
| Solubilidade em acetone | 21.0 g/100 mL |
| Riscos associados | |
| Classificação UE | Tóxico (T) |
| NFPA 704 | |
| Frases R | R20/21/22 R32 R52/53 |
| Frases S | S2 S13 S61 |
| LD50 | 854 mg/kg (oral, rat)[1] |
| Compostos relacionados | |
| Outros aniões/ânions | Cianato de potássio Cianeto de potássio |
| Outros catiões/cátions | Tiocianato de de sódio Tiocianato de amônio |
| Página de dados suplementares | |
| Estrutura e propriedades | n, εr, etc. |
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas |
| Dados espectrais | UV, IV, RMN, EM |
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |
Tiocianato de potássio é o composto químico com a fórmula molecular KSCN. É um sal importante do tiocianato de ânion, um dos pseudo. O composto tem um ponto de fusão baixo em relação à maioria dos outros sais inorgânicos.
Use em síntese química
editarAquoso KSCN quase reage quantitativamente com Pb(NO3)2 para ter Pb(SCN)2, que foi usado para converter os cloreto de acila em tiocianatos.[2]
KSCN converte o carbonato de etileno em sulfeto de etileno.[3] Para este efeito, o KSCN é primeiro fundido sob vácuo para remover a água. Numa reação relacionada, KSCN converte óxido de ciclo-hexeno para o correspondente epissulfido.[4]
- C6H10O + KSCN → C6H10S + KOCN
KSCN é também o produto de partida para a síntese do sulfeto de carbonila.
Outros usos
editarDiluir KSCN aquosa é ocasionalmente usada para efeitos de sangue moderadamente realistas no cinema e teatro. Ele pode ser pintada sobre uma superfície ou mantido como uma solução incolor. Quando em contacto com o cloreto férrico (ou outras soluções contendo Fe3+), o produto da reação é uma solução com uma cor vermelha do sangue, devido à formação do complexo ion thiocyanatoiron. Assim, este produto químico é muitas vezes usado para criar o efeito de "estigmas". Uma vez que ambas as soluções são incolores, elas podem ser colocadas separadamente em cada lado. Quando as mãos entram em contato, as soluções reagir e o efeito parece muito com estigmas . Do mesmo modo, esta reacção é utilizada como um teste para o Fe3+ no laboratório .
Referências
- ↑ http://chem.sis.nlm.nih.gov/chemidplus/rn/333-20-0
- ↑ Smith, P. A. S.; Kan, R. O. (1973). «2a-Thiohomophthalimide». Org. Synth.; Coll. Vol., 5
- ↑ Searles, S.; Lutz, E. F.; Hays, H. R.; Mortensen, H. E. (1973). «Ethylenesulfide». Org. Synth.; Coll. Vol., 5
- ↑ van Tamelen, E. E. (1963). «Cyclohexenesulfide». Org. Synth.; Coll. Vol., 4
