Ácido aspártico
| Ácido aspártico Alerta sobre risco à saúde[1] | |
|---|---|

|
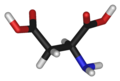
|
| Outros nomes | Ácido 2-aminossuccínico, Ácido 2-amino-butanodioico, Asp |
| Identificadores | |
| Número CAS | ,(enantiômero L) 1783-96-6 (enantiômero D) |
| PubChem | |
| DrugBank | NUTR00016 |
| ChemSpider | |
| Código ATC | V06 |
| SMILES |
|
| Propriedades | |
| Fórmula química | C4H7NO4 |
| Massa molar | 133.08 g mol-1 |
| Ponto de fusão |
270–271 °C (decompõe-se)[1] |
| Solubilidade em água | solúvel (4 g·l-1 a 20 °C)[1] |
| Acidez (pKa) | pKs, α-COOH = 1,99[2] pKs, β-COOH = 3,90[2] pKs, NH2 = 9,90[2] |
| Riscos associados | |
| Frases R | - |
| Frases S | - |
| Compostos relacionados | |
| Aminoácidos relacionados | Ácido aminomalônico (aminopropanodioico) Asparagina (segunda carboxila trocada por amida) Homosserina (4-hidroxi-2-amino-butanoico) Ácido glutâmico (2-aminopentanodioico) |
| Compostos relacionados | Ácido alfa-aminobutírico Ácido málico (hidroxibutanodioico) Ácido succínico (butanodioico) |
| Página de dados suplementares | |
| Estrutura e propriedades | n, εr, etc. |
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas |
| Dados espectrais | UV, IV, RMN, EM |
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |
O ácido aspártico (cuja forma iónica é conhecida como aspartato) é um dos aminoácidos codificados pelo código genético, sendo portanto um dos componentes das proteínas dos seres vivos. É um aminoácido não essencial em mamíferos, tendo uma possível função de neurotransmissor excitatório no cérebro. Como tal, existem indicações que o ácido aspártico possa conferir resistência à fadiga. É também um metabolito do ciclo da ureia e participa na gluconeogénese e pode ser neurotóxico[3].
O aspartato faz também parte do adoçante aspartame.
Metabolismo
editarEm mamíferos, o in vivo a . Este metabolito é também o precursor da síntese do aspartato. A enzima responsável por esta reacção é a aspartato aminotransferase que, como o nome indica, transfere um grupo amina do glutamato para o oxaloacetato para formar aspartato (o outro produto da reacção é o α-cetoglutarato). Este processo ocorre na matriz mitocondrial. O aspartato pode então sair do mitocôndrio e participar no ciclo da ureia, servindo de precursor para o metabolito argininosuccinato. Através deste processo, o aspartato serve de precursor para a síntese de outro aminoácido, a arginina.
O aspartato também serve de precursor na síntese de purinas e pirimidinas. É doador de átomos de azoto, provindos do seu grupo amina, em diferentes passos da síntese de purinas. Na síntese de pirimidinas, o aspartato tem um papel de maior importância, já que oferece o seu esqueleto de carbono como base de construção do anel da base azotada.
As plantas também são capazes de sintetizar aspartato. Após a fixação de CO2 sob a forma de oxaloacetato, este sofre transaminação com um outro aminoácido, originando aspartato e o α-cetoácido correspondente. Algumas plantas usam o aspartato como transportador de CO2; neste caso, a reacção de transaminação inversa ocorre, formando-se oxaloacetato que é depois reduzido a malato (este origina subsequentemente CO2).
Em bactérias, o aspartato origina os aminoácidos metionina, treonina e lisina.
Referências
- ↑ a b c Registo de L-Asparaginsäure na Base de Dados de Substâncias GESTIS do IFA, accessado em 21 de Maio de 2008.
- ↑ a b c Hans-Achim Wagenknecht, Holger Knapp, in: Roempp Online - Version 3.5, 2009, Georg Thieme Verlag, Stuttgart.
- ↑ «Ácido Aspártico - Disciplina - Química». www.quimica.seed.pr.gov.br. Consultado em 6 de março de 2021