Doença de Huntington
A doença de Huntington ou coreia de Huntington é uma doença hereditária que causa a morte das células do cérebro.[4] Os primeiros sintomas são geralmente problemas subtis a nível do humor ou das capacidades mentais.[1] A estes sintomas segue-se falta de coordenação motora e locomoção instável.[2] À medida que a doença avança, começam-se a manifestar movimentos do corpo bruscos, descoordenados e sem sentido.[1] As capacidades físicas vão progressivamente diminuindo até que a coordenação motora se torna difícil e a pessoa se mostra incapaz de falar.[1][2] As capacidades mentais geralmente degeneram em demência.[3] Os sintomas específicos podem variar entre as pessoas.[1] Os sintomas geralmente têm início entre os 30 e 50 anos de idade, mas podem manifestar-se em qualquer idade.[4][3] A cada nova geração, a doença pode-se manifestar cada vez mais cedo.[1] Cerca de 8% dos casos têm início antes dos 20 anos de idade e é comum manifestarem sintomas semelhantes aos da doença de Parkinson.[3] As pessoas com doença de Huntington muitas vezes desvalorizam a gravidade do problema.[1]
| Doença de Huntington | |
|---|---|
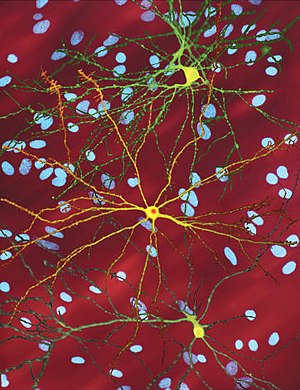
| Imagem microscópica editada de neurónios espinhosos médios (amarelo) com corpúsculos de inclusão (laranja), que ocorrem como parte do processo da doença | |
| Sinónimos | Coreia de Huntington, Mal de Huntington |
| Especialidade | Neurologia |
| Sintomas | Perturbações a nível do humor, capacidades mentais e coordenação motora[1][2] |
| Complicações | Pneumonia, doenças cardiovasculares, lesões físicas por queda, suicídio[3] |
| Início habitual | 30–50 anos de idade[4] |
| Duração | Crónica[4] |
| Causas | Genéticas (herdadas ou nova mutação)[4] |
| Método de diagnóstico | Exames genéticos[5] |
| Condições semelhantes | Coreia de Sydenham, coreia hereditária benigna, lúpus, síndrome paraneoplásica, doença de Wilson[6] |
| Tratamento | Cuidados de apoio[2] |
| Medicação | Tetrabenazina[3] |
| Prognóstico | 15–20 anos após diagnóstico[4] |
| Frequência | 4–15 em cada 100 000 (descendência europeia)[1] |
| Classificação e recursos externos | |
| CID-10 | G10, F02.2 |
| CID-9 | 333.4, 294.1 |
| CID-11 | 2132180242 |
| OMIM | 143100 |
| DiseasesDB | 6060 |
| MedlinePlus | 000770 |
| eMedicine | article/1150165 article/792600 article/289706 |
| MeSH | D006816 |
A doença de Huntington é geralmente herdada de um dos pais, embora em 10% dos casos seja causada por uma nova mutação genética.[1] A doença é causada por uma mutação autossómica dominante em qualquer uma das duas cópias de um gene denominado huntingtina.[4] Isto significa que um filho de uma pessoa com a doença tem 50% de probabilidade de herdar a doença.[4] Este gene fornece a informação genética para uma proteína também denominada "proteína huntingtina".[1] A expansão da repetição do tripleto CAG nesse gene resulta numa forma mutante da proteína, que vai gradualmente destruindo as células no cérebro. No entanto, este mecanismo ainda não é compreendido na totalidade.[4] O diagnóstico é realizado com exames genéticos, que podem ser feitos a qualquer momento, independentemente de existirem ou não sintomas.[5] Esta possibilidade está na origem de alguns debates sobre ética: a idade em que uma pessoa é considerada suficientemente adulta para decidir fazer os exames, se os pais têm o direito de fazer exames nos filhos e como gerir a confidencialidade dos resultados.[2]
Não existe cura para a doença de Huntington.[4] Nos estádios avançados da doença são necessários cuidados a tempo inteiro.[2] O tratamento pode aliviar alguns sintomas e melhorar a qualidade de vida em algumas pessoas.[3] As evidências mais robustas para o tratamento dos problemas de movimento recomendam o uso de tetrabenazina.[3] A doença afeta entre 4 e 15 em cada 100 000 pessoas de ascendência europeia.[1][3] A doença é rara entre japoneses, sendo desconhecida a prevalência entre africanos.[3] A doença afeta mulheres e homens em igual proporção.[3] A esperança de vida é reduzida em resultado de complicações como pneumonia, doenças cardiovasculares e lesões físicas por quedas.[3] Em 9% dos casos a causa de morte é suicídio.[3] A morte geralmente ocorre 15 a 20 anos após o diagnóstico da doença.[4]
A primeira provável descrição da doença foi feita em 1841 por Charles Oscar Waters.[7] No entanto, a primeira descrição detalhada da doença foi feita em 1872 pelo médico George Huntington, de quem tem o nome.[7] A base genética da doença foi descoberta em 1993 por uma colaboração internacional de cientistas coordenado pela Hereditary Disease Foundation.[8][9] A partir da década de 1960 começaram a surgir organizações de apoio e investigação, que trabalham o sentido de aumentar a percepção pública da doença, financiar investigação e oferecer ajuda às pessoas e familiares.[9][10] A investigação atual foca-se na determinação do mecanismo exato da doença, na melhoria dos modelos animais, no ensaio de medicamentos para o tratamento de sintomas ou atraso da progressão da doença, e no estudo de procedimentos como a terapia de células estaminais com o objetivo de reparar os danos causados pela doença.[8]
Causas
editarTrata-se de doença hereditária, causada por uma mutação genética no cromossomo 4. Trata-se de doença autossômica dominante, então se um dos pais tem Huntington, os filhos tem 50% de chances de também desenvolverem a doença. Se um descendente não herdar o gene da doença, não a desenvolverá nem a transmitirá à geração seguinte.
O DNA é constituído de substâncias químicas denominadas nucleotídeos. O indivíduo possuidor dessa desordem apresenta em seu material genético repetições anormais da sequência de bases nitrogenadas citosina, adenina e guanina (CAG), responsáveis pela codificação da glutamina. Numa pessoa sadia a sequência CAG é encontrada com repetições menores que 20; já em pessoas portadoras da doença de Huntington há sempre mais de 36 repetições, tornando assim o gene defeituoso. Estudos recentes indicam que essa região de poliglutamina interfere na interação normal entre uma região rica em glutamina do fator de transcrição chamado Sp1 e uma região rica em glutamina correspondente no "TAFII130", uma subunidade de um componente da maquinaria de transcrição chamado TFIID. Essa interferência dificulta a transcrição nos neurônios do cérebro, incluindo a transcrição do gene para o receptor de um neurotransmissor.[11]
Embora cada célula do corpo tenha duas cópias de cada gene, é suficiente uma cópia do gene anormal para que se tenha esta doença. Então, pode-se dizer que o gene que condiciona a doença de Huntington é um gene dominante.
Sinais e sintomas
editarOs sintomas típicos de Huntigton são[12]:
- Coreia (movimentos involuntários, rápidos, irregulares e sem finalidade dos membros, da face e/ou do tronco, geralmente associados à hipotonia e à diminuição da força muscular);
- Perda progressiva de memória;
- Transtornos psiquiátricos: depressão, ansiedade, irritabilidade, hipersexualidade, egocentrismo.
- Disartria (distúrbios da fala, mastigação e deglutição);
- Fala incompreensível, hesitante, explosiva e desorganizada;
- Perda da visão periférica.
O paciente de DH não morre da doença, mas das complicações oriundas destes sintomas e sequelas instaladas no decorrer da evolução da doença, que é lenta e fatal: tais como fraturas por quedas, desnutrição grave, por não conseguir deglutir, e outras
Diagnóstico
editarO exame genético é determinante. O exame clínico é análise dos sintomas relatados e do histórico familiar da doença. Pode ser diagnosticado por exame genético no feto durante a gravidez.[13]
Prognóstico
editarDesenvolve-se lentamente, provocando uma degeneração progressiva do cérebro, especialmente dos núcleos lenticulares.
A sobrevida varia muito de indivíduo para indivíduo, mas geralmente é de cerca de 10-20 anos após o aparecimento do primeiro sintoma. A morte não é pela doença, mas sim, como consequência de problemas respiratórios (30%) ou cardíacos (25%) causados pela movimentação ineficiente da musculatura, por suicídio (7%) que tem um risco aumentado pelo quadro depressivo ou devido às lesões de quedas frequentes e por má nutrição.
Tem a mesma probabilidade de se desenvolver em ambos os sexos. É muito mais comum entre os descendentes de europeus ocidentais, sendo raro em asiáticos e africanos.
Tratamento
editarNão possui cura, porém possui tratamento sintomático e pesquisas genéticas em primatas estão desenvolvendo uma terapia de silenciamento dos genes causadores da doença.[14] Existem diversos medicamentos para diminuírem os sintomas e o progresso da doença. Exercícios cognitivos diários ajudam a preservar as habilidades mentais reduzindo a perda de memória, percepção e orientação.
Implante de células-tronco
editarEste tratamento tem por base a substituição de neurônios mortos através de uma injeção de células-tronco pluripotentes na área afetada, que ao serem estimulados adequadamente formam novos neurônios, aliviando os sintomas e prolongando a expectativa de vida. Este tratamento já está sendo testado em animais com resultados significativos.[15]
Pesquisa
editarOs pesquisadores, em 2017, descobriram que o tratamento de ratos sem o gene zQ175 heterocigóticos e heterocigóticos de 12 meses de idade por 12 semanas com CTEP, um modulador alostérico negativo do receptor de glutamato metabotrópico 5 (mGluR5), reduziu o tamanho e o número de agregados de huntingtina e também reduziu tanto a apoptose neuronal quanto a perda neuronal no tecido cerebral. Ambos os impedimentos motores e cognitivos foram melhorados nos camundongos ZQ175 tratados com CTEP.[16]
Referências
- ↑ a b c d e f g h i j k Dayalu, P; Albin, RL (fevereiro de 2015). «Huntington disease: pathogenesis and treatment.». Neurologic Clinics. 33 (1): 101–14. PMID 25432725. doi:10.1016/j.ncl.2014.09.003
- ↑ a b c d e f Warby, SC; Graham, RK; Hayden, MR; Pagon, RA; Adam, MP; Ardinger, HH; Wallace, SE; Amemiya, A; Bean, LJH; Bird, TD; Fong, CT; Mefford, HC; Smith, RJH; Stephens, K (2014). «Huntington Disease». PMID 20301482
- ↑ a b c d e f g h i j k l Frank, S (janeiro de 2014). «Treatment of Huntington's disease.». Neurotherapeutics : the journal of the American Society for Experimental NeuroTherapeutics. 11 (1): 153–60. PMC 3899480 . PMID 24366610. doi:10.1007/s13311-013-0244-z
- ↑ a b c d e f g h i j k «Huntington's Disease Information Page: National Institute of Neurological Disorders and Stroke (NINDS)». NINDS. 28 de janeiro de 2016. Consultado em 19 de julho de 2016. Cópia arquivada em 27 de julho de 2016
- ↑ a b Durr, A; Gargiulo, M; Feingold, J (novembro de 2012). «The presymptomatic phase of Huntington disease.». Revue neurologique. 168 (11): 806–8. PMID 22902173. doi:10.1016/j.neurol.2012.07.003
- ↑ Ferri, Fred F. (2010). Ferri's differential diagnosis : a practical guide to the differential diagnosis of symptoms, signs, and clinical disorders 2nd ed. Philadelphia, PA: Elsevier/Mosby. p. Chapter H. ISBN 0323076998
- ↑ a b Vale, TC; Cardoso, F (2015). «Chorea: A Journey through History.». Tremor and other hyperkinetic movements (New York, N.Y.). 5. PMC 4454991 . PMID 26056609. doi:10.7916/D8WM1C98
- ↑ a b «Learning About Huntington's Disease». www.genome.gov. Consultado em 19 de julho de 2016. Cópia arquivada em 4 de julho de 2016
- ↑ a b «History of the HDF». Hereditary Disease Foundation. Consultado em 18 de novembro de 2015. Arquivado do original em 19 de novembro de 2015
- ↑ «Huntington's Disease Society of America – Our History». Huntington's Disease Society of America. 2008. Consultado em 17 de março de 2009. Cópia arquivada em 9 de abril de 2015
- ↑ Andrew SE, Goldberg YP, Kremer B et al. (1993). "The relationship between trinucleotide (CAG) repeat length and clinical features of Huntington's disease". Nat. Genet. 4 (4): 398–403. doi:10.1038/ng0893-398. PMID 8401589.
- ↑ van Duijn E, Kingma EM, van der Mast RC (2007). "Psychopathology in verified Huntington's disease gene carriers". J Neuropsychiatry Clin Neurosci. 19 (4): 441–8. doi:10.1176/appi.neuropsych.19.4.441
- ↑ De Die-Smulders, C. E. M.; De Wert, G. M. W. R.; Liebaers, I.; Tibben, A.; Evers-Kiebooms, G. (2013). "Reproductive options for prospective parents in families with Huntington's disease: Clinical, psychological and ethical reflections". Human Reproduction Update 19 (3): 304–315. doi:10.1093/humupd/dms058. PMID 23377865.
- ↑ McBride JL, Pitzer MR, Boudreau RL et al (25 October 2011). "Preclinical Safety of RNAi-Mediated HTT Suppression in the Rhesus Macaque as a Potential Therapy for Huntington's Disease". Molecular Therapy 19 (12): 2152–2162. doi:10.1038/mt.2011.219. PMC 3242667. PMID 22031240.
- ↑ Cundiff PE, Anderson SA (31 May 2011). "Impact of induced pluripotent stem cells on the study of central nervous system disease". Current Opinion in Genetics & Development 21 (3): 354–361. doi:10.1016/j.gde.2011.01.008. PMID 21277194.
- ↑ mGluR5 antagonism increases autophagy and prevents disease progression in the zQ175 mouse model of Huntington’s disease por Khaled S. Abd-Elrahman et al, publicado em "Sci. Signal" DOI: 10.1126/scisignal.aan6387 (2017)