Corante de Giemsa
Este artigo resulta, no todo ou em parte, de uma tradução do artigo «Giemsa stain» na Wikipédia em inglês, na versão original. |
Coloração ou corante de Giemsa[1] (/ ɡiːmsə /), em homenagem ao químico alemão e bacteriologista Gustav Giemsa, é usado em citogenética e para o diagnóstico histopatológico de malária e outros parasitas.[2]
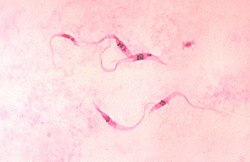

A coloração de Giemsa é um membro do grupo de colorações de Romanowski, que são definidas como sendo o precipitado negro formado pela adição de soluções aquosas de azul de metileno e eosina Y, dissolvidas para o uso em metanol. As variantes do grupo de colorações de Romanowski diferem no grau de oxidação (policromagem) da coloração de azul de metileno antes da precipitação.
A classe de coloração foi originalmente projetada para incorporar coloração citoplasmática (rosa, fruto da eosina Y) com coloração nuclear (azul, dos alterados do azul de metileno) e fixação como um único passo para esfregaços e filmes finos de tecido ( preparações estendidas de omento). Pequenas modificações da concentração de colorações de trabalho e tempo de coloração foram feitas ao longo dos anos para seções de tecidos fixas.
Os pós das misturas corantes das colorações de Romanowski são extremamente tediosas de serem preparadas laboratorialmente, e são melhor adquiridas como corantes de estoque pré-fabricados comercialmente disponíveis.
Usos
editarEla é específica para os grupos fosfato de DNA e se adere a regiões do DNA em que haja grandes quantidades de ligações timina-adenina. O corante Giemsa é usado no bandeamento de Giemsa, comumente chamado de bandeamento G para tingir cromossomos e, muitas vezes usada para criar um cariograma (mapa cromossomo). Ela pode identificar aberrações cromossómicas tais como translocações e rearranjos.
Ele colore o trofozoíto Trichomonas vaginalis, que se apresenta com descarga esverdeada e células móveis em um preparação molhada.[3][4]
A coloração Giemsa é também uma coloração diferencial, tal como quando é combinada com a coloração de Wright para formar a coloração de Wright-Giemsa. Ela pode ser usada para estudar a adesão de bactérias patogénicas às células humanas. Ela marca diferencialmente células humanas, roxas e de bactérias rosa. Ela pode ser utilizada para o diagnóstico histopatológico da malária[5] e alguns outros espiroquetas e protozoários parasitas do sangue. É também utilizada na coloração células Wolbachia em Drosophila melanogaster e Aedes albopictus.[6][7][8][9][10][11]
O corante de Giemsa é um corante de esfregaço de sangue clássico para esfregaços de sangue periféricos e amostras de medula óssea. Os eritrócitos são marcados em rosa, as plaquetas mostram um rosa pálido claro, os linfócitos do citoplasma marcam azul celeste, monócitos do citoplasma azul pálido, e as cromatinas nucleares dos leucócitos magenta. Ele também é usado para visualizar o clássico "pino de segurança" na forma Yersinia pestis.[12]
O corante de Giemsa também é usado para visualizar cromossomos.
O corante de Giemsa o histoplasma do fungo, bactéria clamídia, e pode ser usado para identificar mastócitos.[13]
Colorações características obtidas
editarDiferentes componentes celulares e as colorações características obtidas com corante de Giemsa:[14][15]
| Componente celular | Cor |
|---|---|
| Pigmentos da bile | Verde |
| Colágeno, músculos, ossos | Rosa pálido |
| Microorganismos, fungos, parasitas | Azul purpúreo |
| Grânulos de amido, celulose | Azul celeste |
| Pigmentos (cor nativa sendo amarelo ou castanho, ou se fixada em dicromato contendo fixador) | Verde |
| Núcleos | Azul escuro a violeta |
| Eritrócitos | Rosa salmão |
| Citoplasma | Diferentes tonalidades de azul claro |
Produção
editarA solução de Giemsa é uma mistura de azul de metileno, eosina, e azure B. O corante é geralmente preparado a partir de pó de corante de Giemsa disponível comercialmente.
Formulação da mistura corante
editarAzul de metileno 63,6% em peso, azure B 28,6%, azure A 4,4%, azure C 1,4%, tionina 1,9%. O corante citado “azure I” na publicação original não era um corante “puro”, mas sim uma mistura de tionina e todos os seus derivados 3 e 7-N-metilados. R. D. Lillie inferiu que provavelmente foi preparado por um processo de oxidação ácida.[16]
Técnica de uso
editarUma película fina do espécime numa lâmina de microscópio é fixada em metanol puro durante 30 segundos, mergulhando-a ou colocando algumas gotas de metanol na lâmica. A lâmina é imersa numa solução de corante de Giemsa preparada fresca a 5% durante 20-30 minutos (5-10 minutos em situações de emergência em solução a 10%, podem ser utilizados), em seguida, enxaguada com água da torneira e deixada secar.[17]
Observações técnicas
editarGeralmente a coloração é realizada à temperatura ambiente durante a noite, contudo, o aumento da temperatura da coloração reduz o tempo de coloração. As seções coradas a 37°C durante várias horas (tempo de coloração avaliado por exame microscópico) produzem melhores resultados do que seções coradas a 60°C durante um período mais curto. Quanto maior a temperatura de coloração, maior a intensidade da coloração azul, mas sem a coloração vermelha sendo aumentada equivalente.
A diferenciação com ácido acético variará de acordo com o tempo de coloração e a temperatura, mas é geralmente conseguida em 30 segundos. O agente de diferenciação remove apenas o componente corante azul, aumentando assim a intensidade aparente do componente vermelho.
Uma técnica completa de coloração recomendada é composta das seguintes etapas:
- Desengorduramento em xileno (xilol) - 2 minutos.
- Um segundo desengorduramento em xileno - 2 minutos.
- Um terceiro desengorduramento em xileno - 2 minutos.
- Lavagem em álcool absoluto (etanol anidro) - 2 minutos.
- Uma segunda lavagem em álcool absoluto - 2 minutos.
- Lavagem em álcool (etanol) a 90% - 2 minutos.
- Lavagem em álcool (etanol) a 70% - 2 minutos.
- Lavagem em água corrente - 2 minutos.
- Coloração com corante de Giemsa diluído, recentemente preparado.
- Enxague em água destilada.
- Diferenciação com solução aquosa de ácido acético a 0,5%.
- Lavagem rápida com álcool (etanol) a 70%.
- Lavagem rápida com álcool (etanol) a 95%.
- Lavagem rápida com álcool absoluto.
- Uma segunda lavagem rápida com álcool absoluto.
- Uma terceira lavagem rápida com álcool absoluto.
- Banho de clareamento em xileno - 2 minutos.
- Um segundo banho de clareamento em xileno - 2 minutos.
- Um terceiro banho de clareamento em xileno - 2 minutos.
- Montar as lâminas com cobertura de lamínulas usando DPX, Entellan ou formulação de "bálsamo do Canadá sintético" equivalente.
Ver também
editar- Coloração biológica e protocolos de coloração
- Histologia
- Coloração de Leishman
- Microscopia
- Coloração de Romanowsky
- Coloração de Wright
Referências
- ↑ Lallo, Maria Anete; Eduardo Fernandes. «Stain techniques for detection of Encephalitozoon cuniculi in tissue sections». Ciência Rural. 40 (11): 2406-2410. ISSN 0103-8478. doi:10.1590/S0103-84782010001100027
- ↑ Giemsa G (1904 Eine Vereinfachung und Vervollkommnung meiner Methylenblau-Eosin-Färbemethode zur Erzielung der Romanowsky-Nocht’schen Chromatinfärbung.
- ↑ Razia Khatoon, Noor Jahan, Haris Manzoor Khan, Tamkin Rabbani, and Siraj Ahmad; Evaluation of Different Staining Techniques in the Diagnosis of Trichomonas vaginalis Infection in Females of Reproductive Age Group; J Clin Diagn Res. 2014 Dec; 8(12): DC05–DC08
- ↑ Camila Braz MENEZES, Mariana dos Santos MELLO, Tiana TASCA; COMPARISON OF PERMANENT STAINING METHODS FOR THE LABORATORY DIAGNOSIS OF TRICHOMONIASIS; Rev. Inst. Med. trop. S. Paulo vol.58 São Paulo 2016 Epub Feb 23, 2016.
- ↑ Shapiro HM, Mandy F (setembro de 2007). «Cytometry in malaria: moving beyond Giemsa». Cytometry. Part A : the journal of the International Society for Analytical Cytology. 71 (9): 643–5. PMID 17712779. doi:10.1002/cyto.a.20453
- ↑ Florence Fenollar, Bernard La Scola, Hisashi Inokuma, J. Stephen Dumler, Mark J. Taylor and Didier Raoult; Culture and Phenotypic Characterization of a Wolbachia pipientis Isolate; J. Clin. Microbiol. December 2003 vol. 41 no. 12 5434-5441.
- ↑ Fallon AM; Cytological properties of an Aedes albopictus mosquito cell line infected with Wolbachia strain wAlbB. In Vitro Cell Dev Biol Anim. 2008 May-Jun;44(5-6):154-61. doi: 10.1007/s11626-008-9090-4. Epub 2008 Apr 10.
- ↑ P. G. Hermansa, C. A. Hartb and A. J. Treesa,; In vitro activity of antimicrobial agents against the endosymbiont Wolbachia pipientis; Journal of Antimicrobial Chemotherapy Volume 47, Issue 5Pp. 659-663.
- ↑ CATHERINE PLICHART and ANNE-MARIE LEGRAND; DETECTION AND CHARACTERIZATION OF WOLBACHIA INFECTIONS IN WUCHERERIA BANCROFTI (SPIRURIDA: ONCHOCERCIDAE) VAR. PACIFICA AND AEDES (STEGOMYIA) POLYNESIENSIS (DIPTERA: CULICIDAE); Am J Trop Med Hyg August 2005 vol. 73 no. 2 354-358.
- ↑ Einat Zchori-Fein,Kostas Bourtzis (editado por); Manipulative Tenants: Bacteria Associated with Arthropods; CRC Press, 2011. pg 153.
- ↑ Mark A. Jervis; Insects as Natural Enemies: A Practical Perspective; Springer Science & Business Media, 2007. pg 423.
- ↑ ROBERT D. PERRY AND JACQUELINE D. FETHERSTON; ‘’Yersinia pestis’’ — Etiologic Agent of Plague;; CLINICAL MICROBIOLOGY REVIEWS, 0893-8512/97/$04.0010 Jan. 1997, p. 35–66 Vol. 10, No. 1 - pg 37 e 58.
- ↑ Damsgaard TE, Olesen AB, Sørensen FB, Thestrup-Pedersen K, Schiøtz PO (abril de 1997). «Mast cells and atopic dermatitis. Stereological quantification of mast cells in atopic dermatitis and normal human skin». Arch. Dermatol. Res. 289 (5): 256–60. PMID 9164634. doi:10.1007/s004030050189[ligação inativa]
- ↑ Giemsa's Staining Protocol for Tissue Sections - www.ihcworld.com
- ↑ Giemsa Staining[ligação inativa] - biomedical-sciences.uq.edu.au
- ↑ Perea-Sasiaín J; Giemsa stain's 100th year; Biomedica. 2003 Mar;23(1):5-18.
- ↑ «4.2.2.2. Giemsa stain». impact-malaria.com. Consultado em 28 de outubro de 2013. Arquivado do original em 29 de outubro de 2013