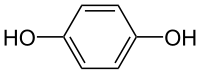
Hidroquinona
Hidroquinona, também chamada benzeno-1,4-diol, 1-4 dihidroxibenzeno ou ainda quinol, é um composto orgânico aromático o qual é um tipo de fenol, tendo a fórmula química C6H4(OH)2. Sua estrutura química tem dois grupos hidroxila ligados a um anel benzênico na posição para. É um sólido granular branco na temperatura e pressão ambiente.
É o isômero 1,4 do benzenodiol, portanto, isômero da resorcina (1,3 benzenodiol) .
Nomenclatura
editarHidroquinona é o nome recomendado pela International Union of Pure and Applied Chemistry (IUPAC) em seu 1993 Recommendations for the Nomenclature of Organic Chemistry [1]
Propriedades
editarHidroquinona pode submetida a oxidação suave converter-se no composto parabenzoquinona, C6H4O2, frequentemente chamado p-quinona ou simplesmente quinona. Redução da quinona reverte esta reação novamente à hidroquinona.
Alguns compostos bioquímicos na natureza que têm este tipo de seção hidroquinona ou quinona em suas estruturas, tais como a coenzima Q, e podem ser submetidas a similares interconversões redox.
Os grupos hidroxila da hidroquinona são completamente ácidos fracos. Hidroquinona pode perder um H+ e uma das hidroxilas para formar um íon monofenolato ou perder um H+ de ambos para formar um íon difenolato.
Usos
editarHidroquinona tem uma variedade de usos principalmente associados com sua ação como um agente redutor sendo solúvel em água. É o principal componente na maioria dos reveladores fotográficos onde, com o composto metol, reduz haletos de prata a prata elementar.
Também é muito usado como inibidor de reações de polimerização de ácido acrílico, metilmetacrilato (acrílico).
Em medicina, hidroquinona é usada como uma aplicação tópica em clareamento da pele ao reduzir a coloração da pele, incluindo clareamento anal, não tendo a mesma predisposição a causar dermatites como o metol faz. Este uso é banido em alguns países (ex.: França) por causa de riscos de câncer.[2][3]
É utilizado no tratamento de melasma.
O sal difenolato de sódio da hidroquinona é usado como um alternativo comonômero na produção do polímero PEEK.
Ela é usada como uma matéria prima de herbicidas, anti-oxidantes para borracha e corantes.
No processamento radiográfico, a hidroquinona é utilizada como agente revelador, reduzindo haleto de prata em prata metálica (negra). É o responsável pelo detalhe da radiografia.
Ocorrência natural
editarÉ uma substância encontrada em vários alimentos, em madeiras, fumo de tabaco, no alcatrão da hulha, óleo cru, etc.
Este composto atua em células produtoras de melanina, os melanócitos, bloqueando a produção e aumentando a degradação dos melanossomos, os corpúsculos intra-celulares que armazenam a melanina. A hidroquinona também bloqueia a ação da enzima tirosinase, que tem participação na formação da melanina.
Referências
editar- ↑ Panico, R.; & Powell, W. H. (Eds.) (1994). A Guide to IUPAC Nomenclature of Organic Compounds 1993. Oxford: Blackwell Science. ISBN 0-632-03488-2
- ↑ Vance, Judi. «The Ugly Side of Beauty» (em inglês). OfSpirit.com. Consultado em 28 de agosto de 2009. Arquivado do original em 25 de março de 2012
- ↑ «Skin bleaching/ lightening & its dangers» (em inglês). pressbox.co.uk. 26 de setembro de 2005. Consultado em 28 de agosto de 2009. Arquivado do original em 25 de março de 2012